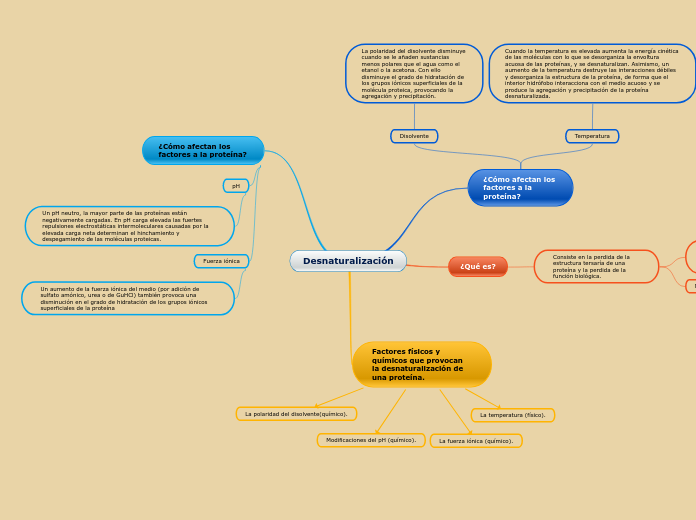
Desnaturalización
¿Cómo afectan los factores a la proteína?
Disolvente
La polaridad del disolvente disminuye cuando se le añaden sustancias menos polares que el agua como el etanol o la acetona. Con ello disminuye el grado de hidratación de los grupos iónicos superficiales de la molécula proteica, provocando la agregación y precipitación.
Temperatura
Cuando la temperatura es elevada aumenta la energía cinética de las moléculas con lo que se desorganiza la envoltura acuosa de las proteínas, y se desnaturalizan. Asimismo, un aumento de la temperatura destruye las interacciones débiles y desorganiza la estructura de la proteína, de forma que el interior hidrófobo interacciona con el medio acuoso y se produce la agregación y precipitación de la proteína desnaturalizada.
¿Qué es?
Consiste en la perdida de la estructura tersaría de una proteína y la perdida de la función biológica.
Provoca un aumento en la entropía de las moléculas trayendo como consecuencia perdidas en estructura secundaria, terciaria y cuaternaria.
No hay cambios en la estructura primaria.
Factores físicos y químicos que provocan la desnaturalización de una proteína.
Modificaciones del pH (químico).
La fuerza iónica (químico).
La temperatura (físico).
La polaridad del disolvente(químico).
¿Cómo afectan los factores a la proteína?
pH
Un pH neutro, la mayor parte de las proteínas están negativamente cargadas. En pH carga elevada las fuertes repulsiones electrostáticas intermoleculares causadas por la elevada carga neta determinan el hinchamiento y despegamiento de las moléculas proteicas.
Fuerza iónica
Un aumento de la fuerza iónica del medio (por adición de sulfato amónico, urea o de GuHCl) también provoca una disminución en el grado de hidratación de los grupos iónicos superficiales de la proteína