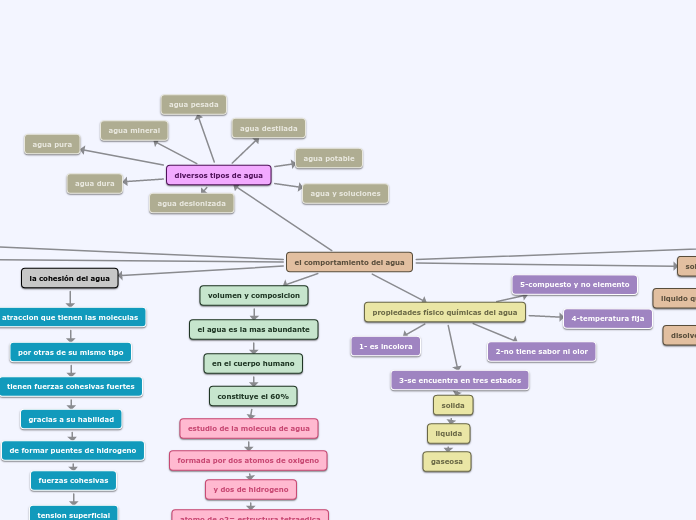
el comportamiento del agua
volumen y composicion
el agua es la mas abundante
en el cuerpo humano
constituye el 60%
estudio de la molecula de agua
formada por dos atomos de oxigeno
y dos de hidrogeno
atomo de o2= estructura tetraedica
atomo de H= orbitales incompletos
forman un enlace covalente
distribucion asimetrica
propiedades físico químicas del agua
1- es incolora
2-no tiene sabor ni olor
3-se encuentra en tres estados
solida
liquida
gaseosa
4-temperatura fija
5-compuesto y no elemento
la cohesión del agua
atraccion que tienen las moleculas
por otras de su mismo tipo
tienen fuerzas cohesivas fuertes
gracias a su habilidad
de formar puentes de hidrogeno
fuerzas cohesivas
tension superficial
tension o estres
la adherencia del agua
tiende a pegarse a si misma
se adhiere a otro tipos de moleculas
adhesión significado
atraccion de moleculas de un tipo
por moleculas de otro tipo
para que el agua sea fuerte
especialmente cuando
tienen cargas positivas y negativas
solubilidad
liquido que mas disuelve
disolvente universal
ionización y el ph
ion hidrogeno
pasa a unirse con el
atomo de oxigeno de la otra molecula
mantenia relaciones
mediante
enlace de hidrogeno
disocia de
átomo de hidrogeno
atomo de oxigeno
el agua es un liquido químicamente puro
solución ionica
el producto se denomina producto ionico del agua
base del ph
mide acidez o alcalinidad
diversos tipos de agua
agua pura
agua mineral
agua pesada
agua destilada
agua potable
agua dura
agua desionizada
agua y soluciones
agua contaminada
debido al agregado de sustancias (impurezas)
alteran su calidad
tres diferentes tipos de impurezas
particulas susprendidas
absorben la luz
el agua se ve turbia y sucia
particulas coloidales
pequeñas
dificiles de retener
particulas disueltas
no se depositan
no son retenida
propiedades fisico quimicas del agua
propiedades que se derivan de su estructura dipolar
capacidad de disolucion
agua= disolvente universal
separacion de moleculas
hace posible los procesos
transporte
nutricion
eliminacion
capacidad de disociación
en moleculas cuyos atomos
unidos por enlaces ionicos
transferencia de puentes de hidrogeno
debilitar
atraccion
y separar
o debilitar sus atomos
sus fuerzas
hidratacion
grupos polares
rodeados por moleculas de agua
en caso de que sean iones
el proceso de hidratacion
salvatacion
modifica caracteristicas fisicas del ion y sus propiedades
disociacion de la propia molecula de agua
agua=electrolito debil
disocia
porcion muy baja
dando un ion hidrogeno
y un ion hidroxilo
propiedades que se derivan de la formacion de puente de hidrogeno
densidad maxima del agua
se obtiene cuando se mide
4°C
agua esta en temperatura liquida
por tanto, el hielo flota
alto calor especifico
1 cal/gramo por °C
grandes cambios de energia termica
modificaciones de temperatura corporal
alto calor de vaporizacion
se puede justificar la eliminacion de grandes cantidades de energia termica
vaporizacion de pequeñas cantidades de agua
temperatura corporal inferior a la ambiental
elevada conductividad termica
agua=transmisor del calor
aparato circulatorio para igualar temperaturas dentro del cuerpo humano
impidiendo que partes del organismo tengan zonas de temperatura
altas
bajas
elevada constante dielectrica
constante 25° C de 78,5
agua en estado puro=buen aislante
conduce mal la corriente electrica
elevada tension superficial
la fuerza de cohesion entre las moleculas de agua da lugar a una elevada
tension superficial
propiedades bioquimicas del agua
disolvente universal
componente estructural
metabolismo intermediario
regulador termico
disoluciones
mezcla homogena
diferentes compuestos
disoluciones=acuosas
dos componentes
soluto
sustancia que disuelve
solvente disolvente
disuelve el soluto
clasificacion de las disoluciones
segun el estado fisico de los componentes
depende de que sean
solidos
liquidos
gaseosos
segun el estado ionico de las moleculas de soluto
moleculas neutras
iones
segun el tamaño de las particulas de soluto
propiedades fisicas
propiedades coligativas
disminucion de la temperatura de congelacion
aumento de la temperatura de ebullicion
descenso de la presion de vapor
presion osmotica
Composición de las disoluciones intracelulares y extracelulares
disoluciones ionicas
membranas plasmaticas
plasma
liquido interstical
liquido intracelular
no son homogeneas