Grupos Funcionales- Juliana & Daniela
Alcoholes
Su grupo funcional es OH y recibe el nombre de Hidroxilo. La prioridad con respecto a los otros tres grupos funcionales que estamos trabajando es la menor de todas en 4to lugar.
Su estructura consiste del grupo Hidroxi (OH) va adjunto a uno de los carbonos, remplazando un Hidrogeno sin dejar de cumplir la tetravalencia. [ R-OH ]
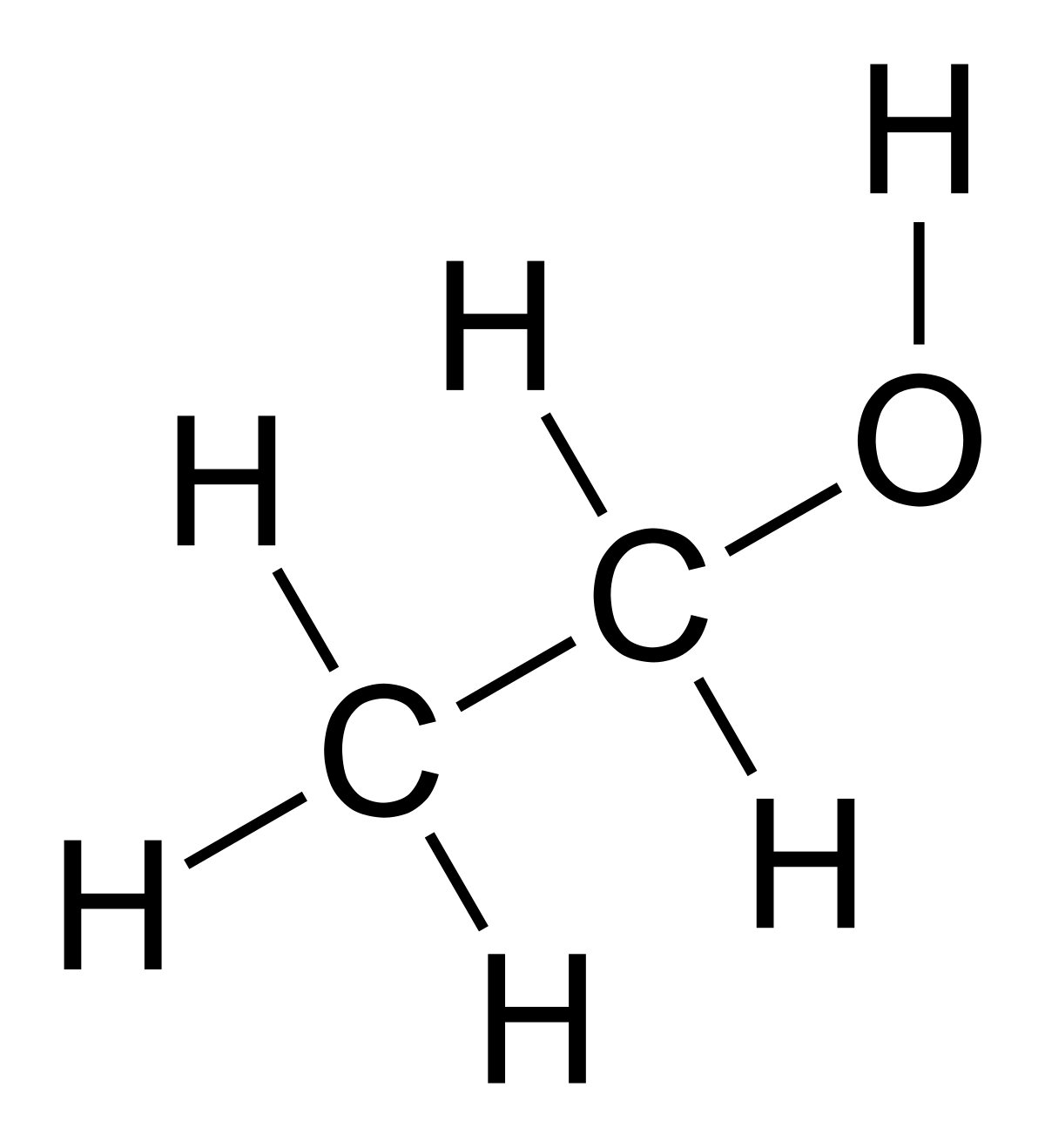
Ejemplo: Etanol (C2H5OH)
Nomenclatura: Para nombrar un alcohol se utiliza el sufijo "-ol" derivado de la palabra alcohol, al final del nombre y después del prefijo de cantidad de Carbonos.
Clasificación según el numero de grupos de hidroxilos
monoalchol o monol: son aquellos que solo tiene un grupo de hidroxilos (-OH)
Ejemplo:
polialcholes: sol los que tienen dos o más grupos de hidroxilos
Ejemplo:
Propiedades Físicas: los alcoholes por lo general son líquidos incoloros que desprenden un olor característico, aunque menos también existen alcoholes en estado sólido, los alcoholes son solubles en agua debido a que su grupo funcional hidroxilo ( -OH) es parecido a la molécula de agua (H2O) y gracias a esto forman puentes de hidrógeno, entre más simple y de menor masa molecular sea el carbono es más soluble en agua, mientras más carbonos tenga el alcohol menos soluble. Su densidad aumenta junto con el número de carbonos y ramificaciones que tenga, finalmente los puntos de fusión y ebullición varían dependiendo del número de grupos hidroxilos y ramificaciones.
Propiedades Químicas: los alcoholes son de carácter dipolar (lo que significa que tienen un polo positivo y uno negativo), pueden comportarse como ácidos o bases dependiendo del reactivo con el que reaccionen (si lo hace con una base fuerte actúa como un ácido, pero si reacciona con un ácido se comportan como una base débil), los alcoholes pueden participar en varias reacciones químicas incluyendo: halogenación, oxidación, deshidrogenación o deshidratación.
Aldehídos

Su grupo funcional es el formilo que consta de un carbono unido a cualquier cadena carbonada de un lado (R) y a una molécula de oxigeno con un enlace doble y a un hidrógeno con un enlace sencillo por el otro lado.(Estructura)
Nomenclatura: se utiliza el el prefijo de cantidad de carbonos seguido del sufijo "-al".
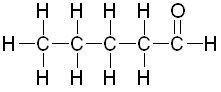
Ejemplo: Pentanal (C5H10O).
Propiedades Físicas: aldehidos de cadenas no mayores de los 4 carbonos son solubles en agua, el punto de ebullición de los aldehidos es mayor al de alíanos de igual masa molecular pero menor al de los alcoholes o ácidos carboxílicos, de uno a dos carbonos son gaseosos, de tres a once son líquidos y de ahí de adelante son sólidos, por lo general desprenden olores profundos y desagradables que disminuyen y se vuelven incluso agradables conforme la masa molecular aumenta.
Propiedades Químicas: son bastante reactivos, ciertos factores que afectan la reactivada de los aldehídos son la intensidad de polaridad ente C y O y el volumen de los agrupamientos enlazados al grupo funcional Formilo, entre menos grupos unidos al formilo con mayor facilidad se genera una reacción gracias al menor impedimento esteárico
Clasificación: los aldehidos pueden ser aromáticos o alifáticos.
Aldehidos Aromáticos: compuestos cuya cadena principal se compone de carbonos e hidrógenos, y el grupo funcional fórmelo ( -CHO) está unido a la cadena de hidrocarburos aromáticos.
Aldehidos Alifáticos: Formaldehído (CH2O) es el único compuesto que contiene 2 átomos de carbono enlazados al grupo formilo.
Cetonas
Las Cetonas se caracterizan por tener un grupo funcional que incluye dos átomos de carbono unidos a uno de carbonilo, respecto a los cuatro grupos funcionales vistos en clase las cetonas ocupan el tercer puesto en cuestión de prioridad.
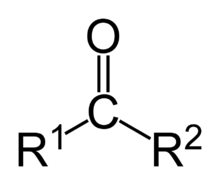
estructura cetonas:
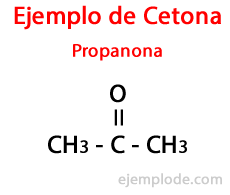
ejemplo de Cetonas
nomenclatura: para nombrara aun Cetona se utiliza al final el sufijo "ona" reemplazando el sufijo "ano" de los Alcanos
Clasificación de las cetonas: esto se debe a los dos radicales hidrocarbonados que se encuentran al lado del carbonilo.
Simétricas: son aquellas donde los radicales al lado del carbonilo son iguales

ejemplo:
Según el tipo de radical hidrocarbonado unido al carbonilo, Las acetonas pueden ser alifáticas, R-CO-R', aromáticas, Ar-CO-Ar, y mixtas; R-CO-Ar.
Asimétricas: cuando los radicales son distintos

ejemplo:
Propiedades Físicas de las acetonas: las cetonas entre 3 y 10 átomos son solubles en agua, con un olor suave , líquidas e incoloras pero cuando tienen más de 10 carbonos se vuelven solidas , Su punto de ebullición es mayor que el de los alcanos de igual peso molecular, pero menor que el de los alcoholes y ácidos carboxílico, y son menos densas que el agua.
Propiedades Químicas:se obtienen por la oxidación de alcholes(alchol secundario) catalizados por agentes químicos, son estables a la oxidación, para reducir las cetonas es un proceso sencillo solo se necesita un catalizador e hidrógeno y al reducirse quedan como un alcohol secundario.
Ácidos Carboxílicos
los ácidos carboxílicos pertenecen al grupo carboxilo (-COOH) y son el producto de la oxidación de los acholes primarios y aldehídos, en su estructura se aprecia que el grupo carboxilo se forma debido a la unión de hidroxilo y carbonilo. Su formula general es R-COOH/Ar-COOH y ocupan el primer puesto de relevancia frente a los otros tres grupos funcionales.


ejemplo de acido carboxílico (ácido fórmico):
nomenclatura: para nombrarlos se se utiliza la terminación "ico" al final del nombre.
Clasificación: se clasifican los ácidos carboxílicos teniendo en cuenta dos simples aspectos, el número de grupos carboxilos que tenga la molécula del ácido.
Monocarboxílicos: la molécula contiene solo un grupo carbonizo. (Fórmula: R-COOH)
Dicarboxílicos: cuando cada molécula contiene dos grupos de carboxilos. (Fórmula: HOOC-CH2(R)-COOH).
Tricarboxílicos: la misma molécula contiene tres grupos funcionales de carboxilo, también son conocidos como ácidos policarboxílicos.
propiedades químicas: los ácidos carboxílicos reaccionan con hidróxidos formando sales de ácidos carboxílicos, las moléculas presentan una geometría trigonal plana y tienen hidrogeno acido en el grupo de los hidroxilos comportándose como bases sobre el oxigeno carboxílico, cuando se separa el acido carboxílico se genera un ión carboxilato con una carga negativa.
propiedades físicas: los ésteres son los derivados mas importantes de los ácidos carboxílicos, estos ácidos se encuentran en variados productos y componentes como, grasas y aceites vegetales , tienen puntos de ebullición superiores a las cetona, alcoholes y aldehídos, son compuestos muy polares y son líquidos hasta 9 átomos de carbono si tienen mas se vuelven solidos.
