Modelo atómico

Estructura Atómica
Ellos afirmaron que la materia esta formada por pequeñas partículas, las cuales llamaron átomo.

Demócrito (460-370 AC) y Leucipo de Mileto (370 AC)
.jpg)
Modelo de John Dalton (1766-1844)

John Dalton (1766-1844)
Reafirmó la teoría de Demócrito y Leucipo, de que el átomo es indivisible.
Modelo atómico de Thomson (1897)
Demostró que dentro de los átomos hay partículas diminutas con carga eléctrica negativa (electrones), dedujo que el átomo es una esfera cargada de materia positiva

Sir Josep John Thomson (1856-1940)
Modelo de Rutherford (1911)

Ernest Rutherford (1871-1937)
Mantuvo que el átomo se compone de una parte positiva y una negativa, sin embargo postula que la carga positiva se concentra en un núcleo, el cual contiene virtualmente toda la masa del átomo. También predijo la existencia del neutrón(1920)

Modelo de Bohr (1913)
Estableció que los electrones giran alrededor del núcleo, describiendo orbitas circulares.

Niels Henrik David Bohr (1885-1962)

Modelo de Goldstein (1914)

Eugen Goldstein (1850-1930)
Con el estudio de rayos canales, determino que estaban formados por partículas con carga positiva y que tenían una masa distinta según cual fuera el gas que estaba encerrado en el tubo.
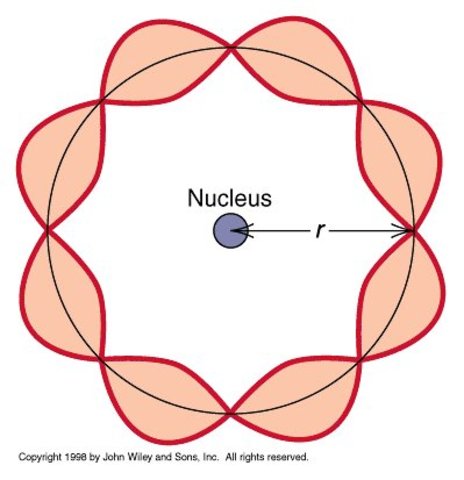
Modelo de L. Broglie (1923)
Louis-Víctor de Broglie (1892-1987)
En 1924 introduce la noción de de los electrones como ondas, presenta por primera ves la Dualidad onda-partícula (no hay diferencia, las partículas pueden comportarse como ondas y viceversa).

Modelo de Schrödinger (1926)
Establece la presencia de orbitales, que son regiones en el espacio (ondas), en donde es probable encontrar al electrón.

Erwin Rudolf Josef Alexander Schrödinger (1887-1961)

Modelo de J. Chadwick (1932)

James Chadwick (1891-1974)
Descubrió la partícula en el núcleo del átomo que pasaría llamarse neutrón. Esta partícula no tiene carga eléctrica.

Modelo de Quarks en los años 60
Murray Gell-Mann (1929-2019) George Zweig (1937-Actualidad)
Corroboraron que dentro de los protones y neutrones habían tres partículas mas pequeñas, a las que llamaron quarks.