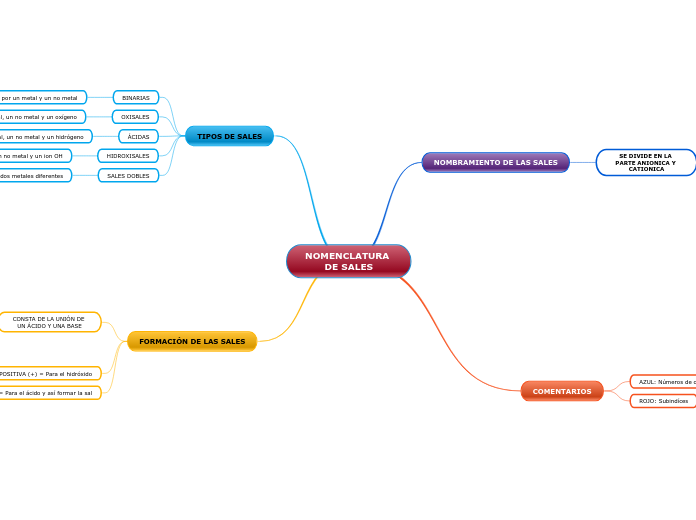
NOMENCLATURA DE SALES
NOMBRAMIENTO DE LAS SALES
SE DIVIDE EN LA PARTE ANIONICA Y CATIONICA
Métodos
Tabla de iones
Sufijos
NOMENCLATURAS
STOCK
TRADICIONAL
EJEMPLOS (TABLA DE IONES)
Na13(PO4)-3
STOCK: Fosfato de sodio (I)
TRADICIONAL: Fosfato sódico
Fe32(SO4)-23
STOCK:Sulfato de hierro (III)
TRADICIONAL: Sulfato férrico
Na-12(CO3)-2
STOCK: Carbonato de sodio (I)
TRADICIONAL: Carbonato sódico
K1(MnO4)-1
STOCK: Perganmanato de potasio (I)
TRADICIONAL: Perganmanato de potasio
EJEMPLOS (SUFIJOS)
OSO=ITO ICO=ATO HÍDRICO= URO
Fe23(P5O-24)-3-2
STOCK: Ferroso de hierro (II)
TRADICIONAL: Fosfato
Na12S6O-24
STOCK: Sulfato de sodio (I)
TRADICIONAL: Sulfato sódico
Fe3Cl-13
STOCK: Cloruro de hierro (III)
TRADICIONAL: Cloruro férrico
COMENTARIOS
AZUL: Números de oxidación
ROJO: Subindíces
TIPOS DE SALES
BINARIAS
Compuestas por un metal y un no metal
MNm
OXISALES
Compuestas por un metal, un no metal y un oxígeno
MNmO
ÁCIDAS
Compuestas por un metal, un no metal y un hidrógeno
MHNm-MHNmO
HIDROXISALES
Compuestas con un metal, un no metal y un ion OH
M(OH)Nm-M(OH)NmO
SALES DOBLES
Compuestos por dos metales diferentes
M-M2-NmO
FORMACIÓN DE LAS SALES
CONSTA DE LA UNIÓN DE UN ÁCIDO Y UNA BASE
Hidróxido + ácido ----> sal + agua
KoH + HCl ----> Kcl + H2O
EJ: HIDRÁCIDA
HCl + Fe (OH)3 ----> Fe Cl3 + H2O
OXÁCIDO
Cu(OH)2 + H2SO4 -----> CuSO4
PARTE POSITIVA (+) = Para el hidróxido
PARTE NEGATIVA (-) = Para el ácido y así formar la sal