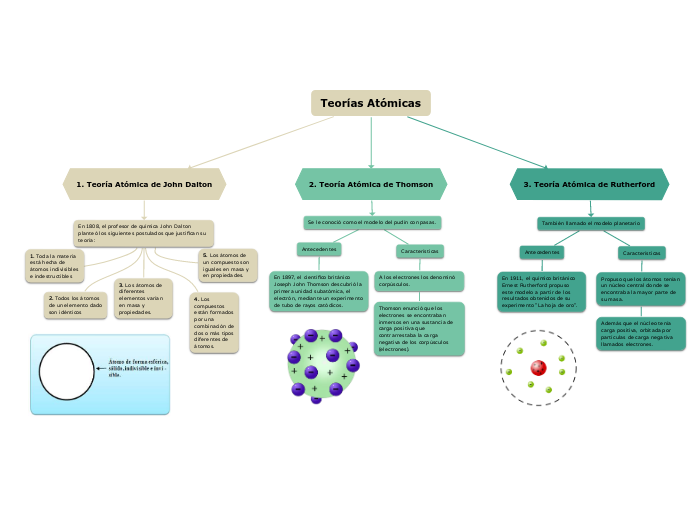
Teorías Atómicas
Teoría Atómica de John Dalton
En 1808, el profesor de química John Dalton planteó los siguientes postulados que justifican su teoría:
1. Toda la materia está hecha de átomos indivisibles e indestructibles
2. Todos los átomos de un elemento dado son idénticos
3. Los átomos de diferentes elementos varían en masa y propiedades.
4. Los compuestos están formados por una combinación de dos o más tipos diferentes de átomos.
5. Los átomos de un compuesto son iguales en masa y en propiedades.
Teoría Atómica de Thomson
Se le conoció como el modelo del pudín con pasas.
Antecedentes
En 1897, el científico británico Joseph John Thomson descubrió la primera unidad subatómica, el electrón, mediante un experimento de tubo de rayos catódicos.
Características
A los electrones los denominó corpúsculos.
Thomson enunció que los electrones se encontraban inmersos en una sustancia de carga positiva que contrarrestaba la carga negativa de los corpúsculos (electrones).
Teoría Atómica de Rutherford
También llamado el modelo planetario
Antecedentes
En 1911, el químico británico Ernest Rutherford propuso este modelo a partir de los resultados obtenidos de su experimento "La hoja de oro".
Características
Propuso que los átomos tenían un núcleo central donde se encontraba la mayor parte de su masa.
Además que el núcleo tenía carga positiva, orbitada por partículas de carga negativa llamados electrones.