por Angie Yuliana Quebrada Garcia hace 3 años
474
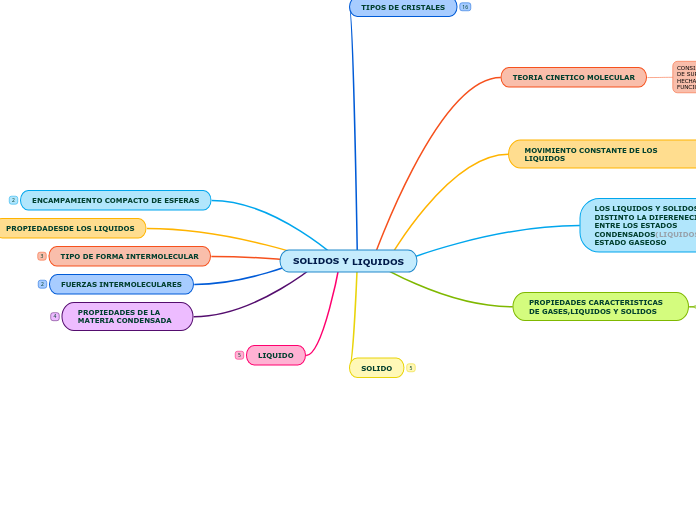
SOLIDOS Y LIQUIDOS
La teoría cinético-molecular explica cómo están hechas las sustancias y cómo interactúan sus moléculas. Destaca que las moléculas están en constante movimiento y que entre ellas existe vacío.