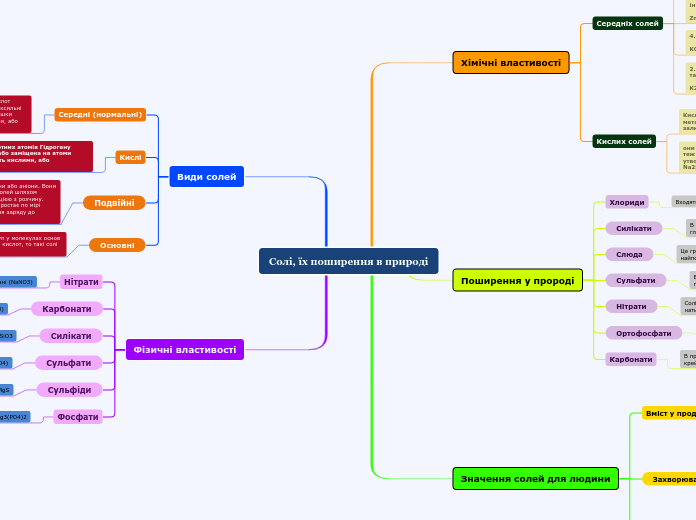
Солі, їх поширення в природі
Хімічні властивості
Середніх солей
1. Взаємодія солі з металом з утворенням іншої солі та іншого металу:
CuSO4 + Fe = FeSO4 + Cu
3. Взаємодія розчинів солей з лугами з утворенням іншої основи та іншої солі:
ZnCl2 + 2NaOH = Zn(OH)2¯ + 2NaCl
4. Взаємодія солей з солями:
KCl + AgNO3 = AgCl¯ + KNO3
2. Взаємодія солі з кислотою з утворенням іншої солі та іншої кислоти:
K2CO3 + H2SO4 = K2SO4 + CO2 + H2O
Кислих солей
Кислі солі у водному розчині дисоціюють на катіони металів, катіони Гідрогену і аніони кислотних залишків. NaOH + H2SO4 = NaHSO4 + H2O
они Гідрогену кислої солі при взаємодії її з основою теж можуть обмінюватись на іони металу з- утворенням нормальної солі і води NaHSO4 + NaOH = Na2SO4 + H2O
Поширення у пророді
Хлориди
Входять до складу мінералів сильвініту та галіту
Силікати
В природі трапляються у формі слюди, горючих сланців, глини
Слюда
Це група мінералів шаруватої будови, з яких найпоширеніші - мусковіт, біотит, лепідоліт.
Сульфати
В природних умовах трапляються як різні кристалогідрати: гіпс, мідний купорос, глауберова сіль.
Нітрати
Солі нітритної кислоти, у природі трапляються рідко. Відомі натьрій, калій, амоній, селітра
Ортофосфати
В природі трапляються в складі фосфоритів та апатитів
Карбонати
В природі трапляються як мінерали мармур, вапняк, крейда.
Значення солей для людини
Вміст у продуктах
Печінка, м'ясо
Горох, курага, какао
Молоко, риба, овочі
Захворювання при нестачі солі
Анемія
Хвороби системи травлення, втомлюваність
Хворои хребта, руйнування зубів
Вплив на людський організм
Входять до складу гемоглобіну
Покращують ріст і міцність кісток
Покращують травлення, роботу головного мозка
Види солей
Середні (нормальні)
Якщо всі кислотні атоми Гідрогену в молекулах кислот обмінені чи заміщені на атоми металів або усі гідроксильні групи в молекулах основ обмінені на кислотні залишки молекул кислот, такі солі називаються нормальними, або середніми, або просто солями.
Кислі
Якщо тільки частина кислотних атомів Гідрогену молекул кислот обмінена або заміщена на атоми металів, такі солі називають кислими, або гідросолями.
Подвійні
складні солі, що містять два різних катіони або аніони. Вони утворюються при взаємодії двох різних солей шляхом твердофазного синтезу або ж кристалізацією з розчину. Ймовірність утворення подвійних солей зростає по мірі збільшення відмінності в іонах відношення заряду до іонного радіуса.
Основні
Якщо тільки частина гідроксильних груп у молекулах основ обмінена на кислотні залишки молекул кислот, то такі солі називають основнимима
Фізичні властивості
Нітрати
Добре розчинні (NaNO3)
Карбонати
Майже всі нерозчинні CaCO3)
Силікати
BaSiO3
Сульфати
Малорозчинні (CaSO4)
Сульфіди
MgS
Фосфати
Mg3(PO4)2