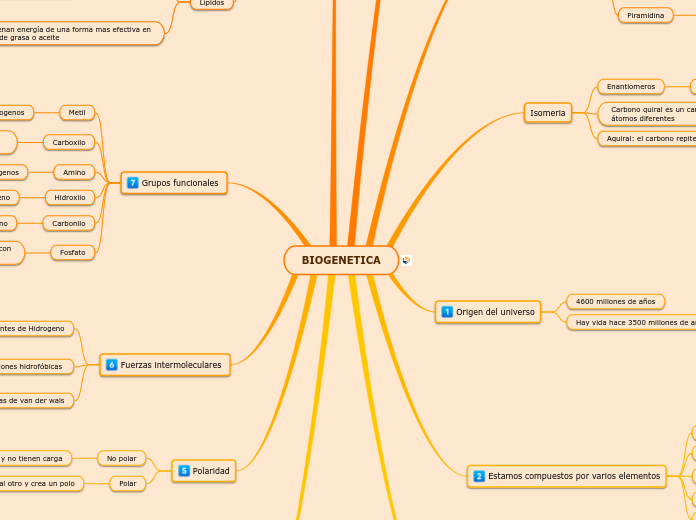
BIOGENETICA
Aminoacidos
Amino, carboxilo y radical
20 aminoacidos
11 no esenciales
Producidos en el organismo
9 esenciales
Adquiridos a través de la dieta
Tipos de estructuras
Primaria
Un amino detrás del otro
Secundaria
Hélice alfa y lámina beta
Terciaria
Fibrosa
Compacta
Globular
Esparcida
Bases nitrogenadas
Nucleótido
Nucleósido+ fosfato
ADN
A-T, G-C- ADN
Timina,citocina, guanina y adenina
ARN
Timina,citocina, guanina y uracilo
U-A - ARN
Purina
Guianina y adenina
Piramidina
Citocina, timina y uracilo
Isomeria
Enantiomeros
Reflejo de una molécula
Carbono quiral es un carbono enlazado a 4 átomos diferentes
Aquiral: el carbono repite un átomo o más
Origen del universo
4600 millones de años
Hay vida hace 3500 millones de años
Estamos compuestos por varios elementos
Oxígeno
Carbono
Azufre y fosforo
síntesis de proteínas
Hidrogeno
Nitrogeno
Bioelementos
Secundarios
Na
Ca
K
Mg
Cl
Oligoelementos
Fe
Zn
F
Mn
Cu
8. Biomoleculas
Carbohidratos
Energía fugaz
Proteínas
Molecula más compleja y de mayor tamaño
Hormonas que transmiten información entres las celulas
Transporte de oxigeno por la hemoglobina (Transporte y almacenamiento de otras moléculas más pequeñas)
Son el ultimo recurso para obtener energía
Catalizadoras
Ácidos nucleicos
Poseen la información que dicta la estructura de las moléculas de proteínas del organismo
Lípidos
Fosfolipidos
Glicolípidos
Compuesto que contiene uno o más residuos monosacáridos unidos
Componentes estructurales de ls membrana celular
Almacenan energía de una forma mas efectiva en forma de grasa o aceite
Grasas cis
Son buenas porque son más flexibles
Grasas Trans
Malas para el organismo por tener enlaces más fuertes
Grupos funcionales
Metil
Carbono unido a tres hidrogenos
Carboxilo
Carbono unido en un doble enlace con un oxigeno y un hidroxilo
Amino
Nitrógeno unido a dos hidrógenos
Hidroxilo
Oxigeno unido a un hidrogeno
Carbonilo
Carbono y doble enlace al oxígeno
Fosfato
Fosforo unido a cuatro oxígenos, uno de ellos con doble enlace
Fuerzas intermoleculares
Puentes de Hidrogeno
Enlace de H entre un átomo e- (interacción de N y H) Solo hay puente de hidrogeno cuando hay presencia de hidrógenos
Interacciones hidrofóbicas
Interacciones que repelen lo no polar (agua y aceite)
Fuerzas de van der wals
Cuando no interactúa ni oxigeno ni nitrógeno y son muy débiles
Polaridad
No polar
Se complementan y no tienen carga
Polar
Un átomo arrastra al otro y crea un polo
Tipos de enlace
Enlace covalente
No covalente
Se rompes y se forman fácilmente porque no tienen mucha energía
Dos átomos no metálicos se unen y comparten uno o más electrones de su último nivel
Enlace doble y triple
Doble: comparte un par de electrones y el triple: comparte tres pares de electrones
Regla del octeto
Dioses de la perfección y estabilidad
Enlace iónico
Unión de dos iones con carga opuesta (el metal cede electrones al no metal)