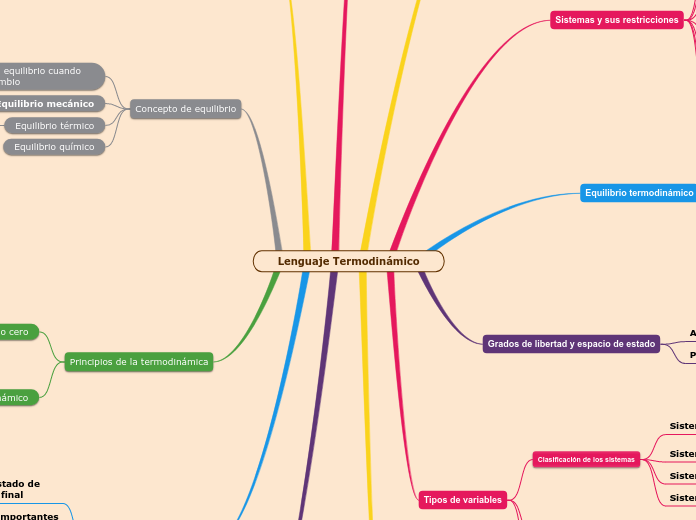
Lenguaje Termodinámico
Termodinámica
ciencia fenomenológica
o ciencia macroscópica
Estructura atómicas y molecular de la materia
Sistemas y sus restricciones
Sistemas termodinámicos
Esta constituido por materia y radiación
Lo conforma paredes de recipiente y paredes exteriores
Alrededores
Caracterizada por intercambios de masa y energía
El grado de interacción dependerá de la naturaleza de sus paredes
Paredes adiabáticas
No se modifica su grado de calentamiento
Paredes diatémicas
Se puede modificar el grado relativo de calentamiento
Sistema cerrado
No pueden intercambiar materia con sus alrededores
La masa permanece constante
Sistema abierto
Intercambio de materia de energía con sus alrededores
Sistema aislado
No tiene interacción con su alrededor
Equilibrio termodinámico
Sistema macroscópicos
Son valores numéricos
Alcanza un estado de equilibrio
Grados de libertad y espacio de estado
Atributos medibles
Limitaciones geométricas
largo , ancho y volumen
Propiedades mecánicas
Presión y tensión
Grados de libertad de un sistema
Tipos de variables
Clasificación de los sistemas
Sistema abierto
La materia ,el calor y el trabajo pueden atravesar libremente
Sistema cerrado
Impide el pasaje de materia
Permite el pasaje de materia y calor
Sistema adiabático
Permite el pasaje de trabajo
Impide el pasaje de calor y materia
Sistema aislado
Impide el pasaje
materia , calor y trabajo
Variables intensivas
Son independientes de la tensión
Como la presión y densidad
Variables extensivas
Resultan aditivas de energía y volumen
Propiedades del sistema
Dependen de las condiciónes de la medida
Propiedades extensivas
Dependen del tamaño del sistema
Cuando se unen obtienen el valor total
Se utilizan letras mayúsculas
Propiedades intensivas
Son independientes del tamaño del sistema
Por ejemplo viscosidad ,altura ,presión temperatura
Proceso de casi-equilibrio
Cambia de valor uan variable de estado
Concepto de proceso
Cambio de estado desde un estado inicial hasta un estado final
Concepto de equilibrio
Un sistema esta en equilibrio cuando no tiene ningún cambio
Equilibrio mecánico
Ninguna fuerza desequilibrada
Equilibrio térmico
Ninguna diferencia de temperatura
Equilibrio químico
Principios de la termodinámica
Principio cero
Fue formulado por primera vez Ralph H Fowler
Ley aplicada para sistemas en equilibrio térmico
Sistema termodinámico
Sistema macroscópico
Comprende la posición y velocidad de partículas
Procesos Termodinámicos
Transcurre desde un estado de equilibrio inicial a otro final
Procesos más importantes
Isotérmicos
A temperatura constante
Isobárico
A presión constante
Isocórico
A volumen constante
Adiabático
No intercambia calor con su entorno
Sistemas Homogéneos y Heterogéneos
Sistema Homogéneos
Presenta un solo estado
Solido ,liquido ,gaseoso ,solución
Sistema heterogéneos
Cuando el sistema presenta dos o mas faces homogéneas en su conformación