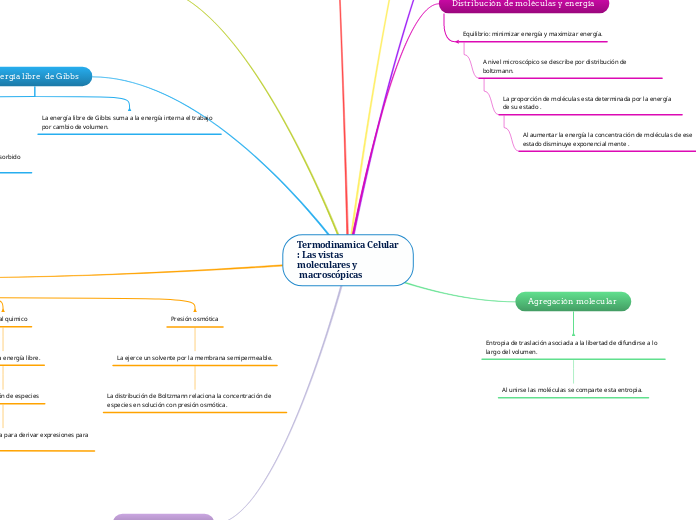
Termodinamica Celular
: Las vistas
moleculares y
macroscópicas
Tensión superficial
Energía libre entre moléculas de agua de la superficie y las del interior.
Se realiza trabajo al introducir una molécula a la superficie.
Equilibrios
Presión osmótica
La ejerce un solvente por la membrana semipermeable.
La distribución de Boltzmann relaciona la concentración de especies en solución con presión osmótica.
Potencial quimico
Medida de la energía libre.
concentración de especies
Termodinamicamente se utiliza para derivar expresiones para potencial químico.
Equilibrio de fases
Equilibrio entre liquido-vapor, o solido-liquido.
Los conceptos termodinámicos describen la distribución molecular.
Electroquimicos
Entre especies ionicas. Se basan en la distribución de Boltzmann.
Relaciona el potencial eléctrico de una celda electroquimica con la concentración de iones.
Energía libre de Gibbs
La energía libre de Gibbs suma a la energía interna el trabajo por cambio de volumen.
Proceso a temperatura constante.
El calor generado se transfiere a otro sistema y el absorbido llega de los alrededores.
Entalpia
La energía necesaria la proporcionan las moléculas.
Para cambiar el volumen se requiere un trabajo.
H= energia interna + presion x volumen
H=U + PV
Equilibrio
Tomando en cuenta la transferencia de calor y otras formas de energía.
Esta diferencia se formaliza como entropia.
Transferir una cantidad de calor a temperatura, el sistema aumenta la entropia .
La energía se adquiere de fuentes de baja entropia (luz solar y alimentos) y la utiliza en mecanismos bioquímicos, fisiológicos y ecológicos.
Luz visible, UV, son energía útil.
Energía irradiada por organismos .
La tierra es un estado estacionario.
Estado estable, siempre tendrá la misma energía y materia.
Termico, se mantiene a la misma temperatura.
Agregación molecular
Entropia de traslación asociada a la libertad de difundirse a lo largo del volumen.
Al unirse las moléculas se comparte esta entropia.
Distribución de moléculas y energía
Equilibrio: minimizar energía y maximizar energía.
A nivel microscópico se describe por distribución de boltzmann.
La proporción de moléculas esta determinada por la energía de su estado .
Al aumentar la energía la concentración de moléculas de ese estado disminuye exponencial mente .
La distribución es consecuencia de interacción entre energía térmica y entalpia.
Alta entropia implica distribución homogénea de moléculas en todo el sistema.
Baja energía de moléculas en estado de menor energía.
Equilibrio termodinámico es minimizar energía y maximizar entropia.
Termodinamica celular
Mide temperatura, presión, tensión de membrana, etc.
La mecánica estadística estudia el comportamiento de muchas cantidades y deduce el comportamiento microscópico.
Relaciona termodinámica con leyes newtonianas o cuantum mecánico a nivel molecular.
Se puede pasar de estado improbable (números pequeños) a probable ( números grandes) .
Aplica a sistemas sin conocer detalles moleculares.
Distribución de Boltzmann
Comprende las propiedades termodinámicas del sistema.
Distribución de probabilidad que describe distribución entre moléculas con diferentes estados de energia en un sistema de equilibrio.