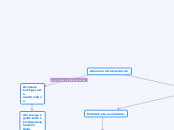
Atomoen arteko loturak
Atomoen konfigurazio elektronikoa
Oro har, gas geldo baten konfigurazia hartzen dute.
Gas geldoen egonkortasuna lortzeko elektroiak galdu, hartu ala irabazi egiten dute, balentzia-geruza beteta izateko 8 elektroiekin.
Hori zortzikotearen araua da.
hauen artean gertatzen dira
Metalak eta ez metalak
Sare (kristal) ionikoak
Lotura ionikoa
Elektroien transferentzia
Ioiak ala katioiak sortzen dute zortzikotearen araua betetzeko.
ionizazio erreakzioen bidez azaltzen da.
Haien propietateak hauek dira:
Fusio- eta irakite-tenperaturak altual edo oso altuak dira.
Kristal ionikoak gogorrak izaten dira.
Hauskorrak dira.
Konposatu ioniko asko disolbatzaile polarretan disolba daitezke.
Bakarrik likido egoeran elektrizitatearen eroaleak dira.
Solidoak dira.
Ez mrtalak eta ez metalak
Molekulak
Kristal kobalenteak
Lotura kobalentea
Elektroien partekatzea
Elektroiak partekatzen dute, zortzikotearen araua betetzeko.
Lewis-en adierazpenarekin azaltzen da
Haien propietateak hauek dira
Solidoak dira.
Fusio- eta irakite-tenperaturak altuak.
Oso gogorrak dira.
Ez dira elektrizitatearen eroale onak.
Elementu bereko metalen atomoak
Sare (krital) metalikoak
Lotura metalikoa
Balentzia elektroiak
Elektroi-hodeiaren eredua
Subtema
Haien propietateak hauek dira:
Dentsitate handia dute.
Fusio-tenpretura altua dute.
Oso gogorrak dira.
Oso harikorrak eta xaflakorrak dira.
Eroankortasun elektriko handia dute.
Disolbagarriezinak dira.
Disdira metalikoa dute.