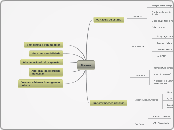
Gases
Sem forma e volume fixos
Alta compressibilidade
Alta capacidade de expansão
Alto grau de liberdade molecular
Variáveis de estado
Pressão (P)
Relação entre força e área
É de 1 atm no nivel do mar
Dado em atm
Volume (V)
Relação entre espaço e matéria
O volume do recipiente é o mesmo volume do gás
O gás ocupa todo o recipiente
É dado em m³
Temperatura (T)
É a agitação termica das moléculas
Dado em Kelvin
Dado em Kelvin(k)
1k=273Cº
Transformações gasosas
Isotérmica
Temperatura constante
P.V=T (constante)
A pressão e o volume são inversamente proporcionais
Isocórica/isovolumétrica
Volume constante
P/T=V (constante)
Pressão e temperatura são diretamente proporcionais
Isobárica
Pressão constante
V/T=P (constante)
Volume e temperatura são diretamente proporcionais
Equação geral dos gases
P1*V1/T1=P2*V2/T2