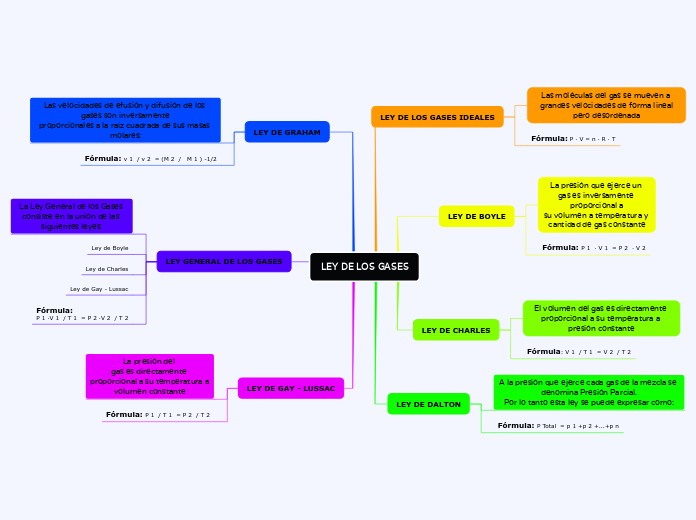
LEY DE LOS GASES
LEY DE LOS GASES IDEALES
Las moléculas del gas se mueven a grandes velocidades de forma lineal
pero desordenada
Fórmula: P · V = n · R · T
LEY DE BOYLE
La presión que ejerce un gas es inversamente proporcional a
su volumen a temperatura y cantidad de gas constante
Fórmula: P 1 · V 1 = P 2 · V 2
LEY DE CHARLES
El volumen del gas es directamente proporcional a su temperatura a presión constante
Fórmula: V 1 / T 1 = V 2 / T 2
LEY DE DALTON
A la presión que ejerce cada gas de la mezcla se denomina Presión Parcial.
Por lo tanto esta ley se puede expresar como:
Fórmula: P Total = p 1 +p 2 +...+p n
LEY DE GRAHAM
Las velocidades de efusión y difusión de los gases son inversamente
proporcionales a la raíz cuadrada de sus masas molares:
Fórmula: v 1 / v 2 = (M 2 / M 1 ) -1/2
LEY GENERAL DE LOS GASES
La Ley General de los Gases consiste en la unión de las siguientes leyes:
Ley de Boyle
Ley de Charles
Ley de Gay - Lussac
Fórmula:
P 1 ·V 1 / T 1 = P 2 ·V 2 / T 2
LEY DE GAY - LUSSAC
La presión del gas es directamente proporcional a su temperatura a volumen constante
Fórmula: P 1 / T 1 = P 2 / T 2