Seguridad en el laboratorio
Número CAS y Número UN
El número de tarjeta de identidad de las Naciones Unidas o de las Naciones Unidas es un número de cuatro dígitos que representa sustancias y artículos peligrosos.
Por ejemplo la acrilamida se identifica con el UN2074

El número de registro CAS es una identificación numérica única para compuestos químicos
Frases R y frases S
Frases R
R1 – Explosivo en estado seco.
R2 – Riesgo de explosión por choque, fricción, fuego u otras fuentes de ignición.
R3 – Alto riesgo de explosión por choque, fricción, fuego u otras fuentes de ignición.
R4 – Forma compuestos metálicos explosivos muy sensibles.
R5 – Peligro de explosión en caso de calentamiento.
R6 – Peligro de explosión, en contacto o sin contacto con el aire.
R7 – Puede provocar incendios.
R8 – Peligro de fuego en contacto con materias combustibles.
R9 – Peligro de explosión al mezclar con materias combustibles.
R10 – Inflamable.
Frases S
S 1 – Consérvese bajo llave.
S 2 – Manténgase fuera del alcance de los niños.
S 3 – Consérvese en lugar fresco.
S 4 – Manténgase lejos de locales habitados.
S 5 – Consérvese en … (líquido apropiado a especificar por el fabricante).
S 6 – Consérvese en … (gas inerte a especificar por el fabricante).
S 7 – Manténgase el recipiente bien cerrado.
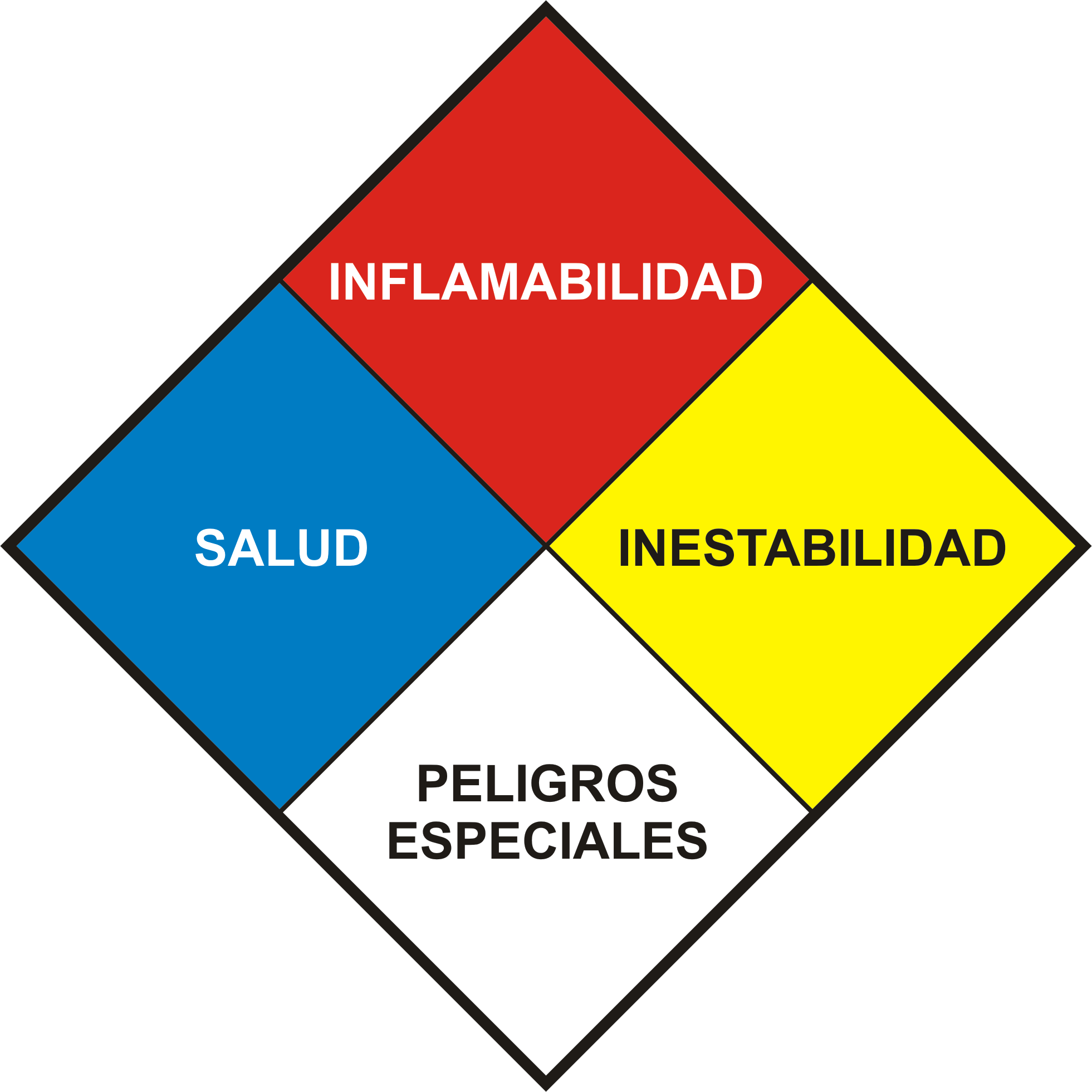
Norma NFPA 704

RIESGO DE INFLAMABILIDAD:
0.No arde
1. Arde a más de 93°c
2. Arde a meno de 93°c
4. Arde a menos de 37°c

PELIGRO PARA LA SALUD:
0. Normal
1. Poco peligro
2. Peligroso
3. Muy peligroso
4. Mortal

RIESGO POR READEACTIVIDAD:
0. Estable
1. Inestable
2. Cambio químico violento
3. Puede explotar por choque o calentamiento
4. Puede explotar

PELIGRO ESPECÍFICO:
Inflamable
No usar aggua
Tóxico
Radiactivo
Corrosivo
Oxidante
Ácido
Alcalino
SOLUBILIDAD Y MISCIBILIDAD
SOLUBILIDAD
Es la capacidad de una sustancia para disolverse en otro llamado solvente. También se refiere a la masa de un soluto que se puede disolver en un solvente de cierta masa bajo ciertas condiciones de temperatura e incluso presión (en el caso de un soluto gaseoso)
LA FASE
Es una parte del sistema, que es microscópicamente uniforme de acuerdo con sus propiedades físicas y químicas, y está separada de otras partes similares por regiones limítrofes bien definidas (llamadas interfaces).
LA FASE LÍQUIDA de una sustancia, que se basa en agua líquida, como una solución de una sustancia en agua. Hablamos de soluciones acuosas, siempre que el disolvente (o la mayoría de los disolventes, en el caso de disolventes mixtos) sea agua. Como solvente, el agua es muy polar y forma fuertes enlaces de hidrógeno.
FASE ORGÁNICA:disolventes orgánicos o disolventes inmiscibles con agua.
SOLUCIÓN
Este es el resultado de la mezcla entre el soluto (es decir, la sustancia que se disuelve) y el solvente (la sustancia en la que se disuelve el soluto).
CLASIFICACIÓN
DE COMPUESTOS
ORGÁNICOS
En general cuatro tipos de compuestos son solubles en agua, los electrolitos, los ácidos, las bases y los compuestos polares. Los electrolitos, las especies iónicas se hidratan debido a las interacciones ión-dipolo entre las moléculas de agua y los iones.
MISCIBILIDAD
Es un término utilizado en química, que se refiere a la propiedad de que ciertos líquidos se mezclan en cualquier proporción para formar una solución. En principio, el término también se aplica a otras fases (sólidos, gases), pero se usa más comúnmente para indicar la solubilidad de un líquido en otro líquido.
FUERZAS INTERMOLÉCULARES
En una molécula, los átomos están conectados por fuerzas intramoleculares (principalmente iones, metales o enlaces covalentes). Estas son las fuerzas que deben superarse para que se produzcan cambios químicos. Por tanto, son estas fuerzas las que determinan las propiedades químicas de la materia.