FUNCIÓN QUÍMICA

QUÍMICA ORGÁNICA
SE FUNDAMENTA EN:

CARBONO

OXIGENO
HIDROGENO

NITROGENO

COMPUESTOS QUIMICOS
Sustancias formadas por interacción con mas de un atomo
COMBINACIONES QUIMICAS
Una sustancia se transforma en otra, produciendo modificaciones en la estructura atómicas molecular llamadas productos de la reacción
ECUACION QUIMICA
REACCION PRODUCIDA
SIMBOLOGIA ADECUADA
NOMECLATURA
Reglas o formulas para nombrar los compuestos quimicos (IUPAC)
SUD INDICE
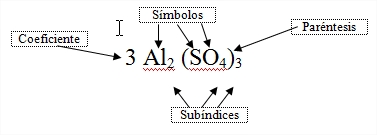
Solo multiplican lo que se encuentran a su izquierda
COEFICIENTE
Multiplican todo lo que se encuentre a su derecha hasta el proximo signo
CLASIFICACION DE COMPUESTOS QUIMICOS
METALES Y NO METALES CON OXIGENO Y CON HIDROGENO
BINARIOS
SON FORMADOS POR DOS TIPOS DE ATOMOS (CARBONO E HIDROHENO)

HIDROCARBUROS
CICLOS
TERNARIO
HETEROCICLOS (algun atomo distinto al C en los ciclos)
CICLOALQUENOS (doble ligadura)
CICLOALCANOS (cadena simple)
ISOCICLICOS (solo carbono)
ALIFÁTICOS
INSATURADOS
ACETILENICA (triple ligadura)
ETILENICA (doble ligadura)
SATURADOS
FORMENICOS (ligadura simple)
TERNARIOS
COMBINACION BINARIO + OXIGENO

AZUFRADOS
TIOSTERES
TIOLES (reemplazan el oxigeno de los alcoholes por el azufre)

OXIGENADOS
SIMPLES
ALCOHOLES (uno o mas oxhidrilos)
ALDEHIDOS (posee un grupo de carbonilo)
CETONAS (un grupo de carbolino pero sobre un carbon secundario)
ACIDOS (poseen varios grupos de carboxilo)
DERIVADOS
ACETALES (combinacion de dos alcoholes con un carbonilo)
ANHIDRIDOS (son el producto de la reaccion de acido con perdida de una molecula de agua)
ESTERES (combinacion de un alcohol + un acido produciendo deshidratacion)
ETERES (combinacion de dos alcoholes con perdida de una molecula de agua)
CUATERNARIOS

COMPUESTOS TERNARIOS + NITROGENO O FOSFORO

OXIDOS BASICOS
COMBINACION METALES + OXIGENO
Ca + O = OXIDO DE CALCIO
ISOMERIA
SUS COMPONENTES PRESENTAN LA MISMA FORMULA MOLECULAR PERO DIFERENTES PROPIEDADES FISICAS QUIMICAS O BIOLOGICAS
ISOMERIA OPTICA
ISOMERIA GEOMETRICA
ISOMERIA CONFORMACIONAL
ISOMERIA ESPACIAL
ISOMERIA PLANA

MOL
PESO MOLECULAR EXPRESADO EN grs
TEMPERATURA Y PRESIÓN Vol molar = 22.4 Litros
ES LA CANTIDAD QUE CONTIENE EL NUMERO DE MOLECULAS
HIDRUROS
H2 + METAL
SE INTERCAMBIAN VALENCIAS
ESTEQUIOMETRIA
Establece y regula las relaciones cuantitativas entre las sustancias que intervienen, análisis y reacciones químicas

HIDROCARBUROS BENCENICOS O AROMATICOS
COMPUESTOS PROVENIENTES DE FUENTES NATURALES
SALES NEUTRAS
RADICAL + MATAL (valencias compensadas)
SALES ACIDAS
RADICAL + HIDROGENO + METAL (sus terminos se pueden restar)

SALES BASICAS
RADICAL + OXIDRILO + METAL son sales que poseen uno o mas oxhidrilos (HO)
RADICALES Estructuras con valencias libres, que permiten combinarse con estructuras semejantes
HIDROXIDOS
OXIDO BASICO + AGUA
SALES
ACIDO + BASE A SAL + H2O ( HIDROXIDO + OXACIDOS (OXISAL) + H2O
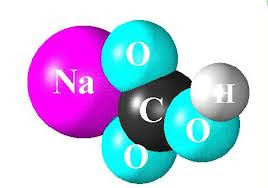
OXACIDOS
COMBINACIÓN OXIDO ACIDO + MOLECULA DE AGUA
CO2 + H2O = CO3H2 ACIDO CARBONICO
NOMETALUROS DE HIDROGENO
NO METAL + HIDROGENO
SiH4 (SILICIO CON HIDROGENO)
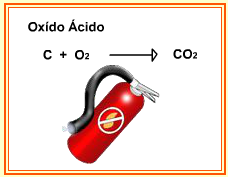
OXIDOS ACIDOS O ANHIDRIDOS
COMBINACIÓN NO METAL + OXIGENO
C + O = ANHIDRIDO CARBONOSO O MONOXIDO DE CARBONO

HIDRACIDOS
ACIDOS DISUELTOS EN AGUA
HALOGENOS