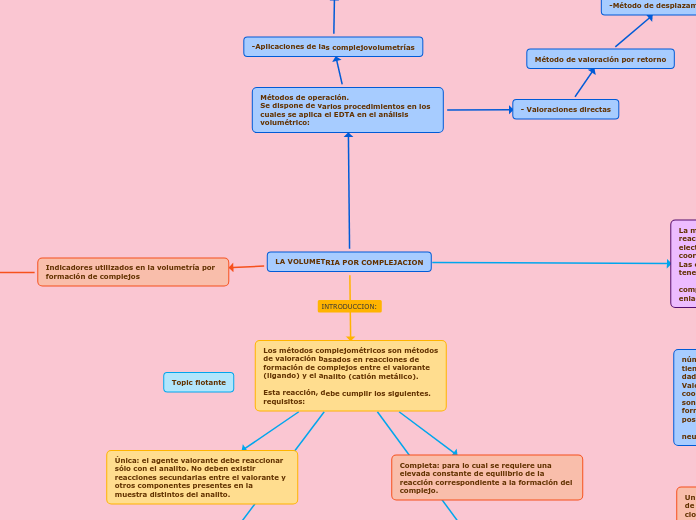
LA VOLUMETRIA POR COMPLEJACION
Los métodos complejométricos son métodos de valoración basados en reacciones de
formación de complejos entre el valorante (ligando) y el analito (catión metálico).
Esta reacción, debe cumplir los siguientes. requisitos:
Indicadores utilizados en la volumetría por formación de complejos
Los indicadores utilizados en la volumetría por formación de complejos son compuestos
orgánicos que forman quelatos coloreados con el átomo metálico (analito), fácilmente
detectables en un rango de concentraciones 10-6-10-7 M y se llaman indicadores
metalocrómicos. Estos indicadores (In) presentan diferentes colores cuando se
encuentran en su forma complejada (color1) y en su forma libre (color2).
La reacción de formación del complejo metal-indicador debe ser rápida y
selectiva.
La intensidad de los colores debe ser elevada de manera que sea sensible a
pequeñas concentraciones de metal.
El complejo metal-indicador debe ser estable, pero menos estable que el
complejo formado entre el metal y el EDTA, para que ocurra rápidamente la
reacción de desplazamiento.
Tanto el indicador como el complejo con el metal deben ser solubles en agua.
Métodos de operación.
Se dispone de varios procedimientos en los cuales se aplica el EDTA en el análisis
volumétrico:
- Valoraciones directas
Método de valoración por retorno
-Método de desplazamiento
Subtopic
-Aplicaciones de las complejovolumetrías
Las titulaciones con EDTA poseen muchas aplicaciones en las ciencias agrarias y
forestales, por ejemplo, la determinación del contenido de calcio y magnesio en aguas
es un análisis de rutina en los laboratorios. Este tipo de valoraciones es también
empleado para analizar la composición de los alimentos (previo tratamiento de las
muestras) en los laboratorios de análisis bromatológico. Otra de sus aplicaciones es la
determinación de Ca2+ y Mg2+ en plantas, ya que son dos nutrientes importantes para el
crecimiento y desarrollo vegetal. Cabe recordar que el punto de partida para poder
utilizar el EDTA como agente valorante es tener una solución de concentración conocida.