da Hernández Pineda Hernández Pineda mancano 4 anni
417
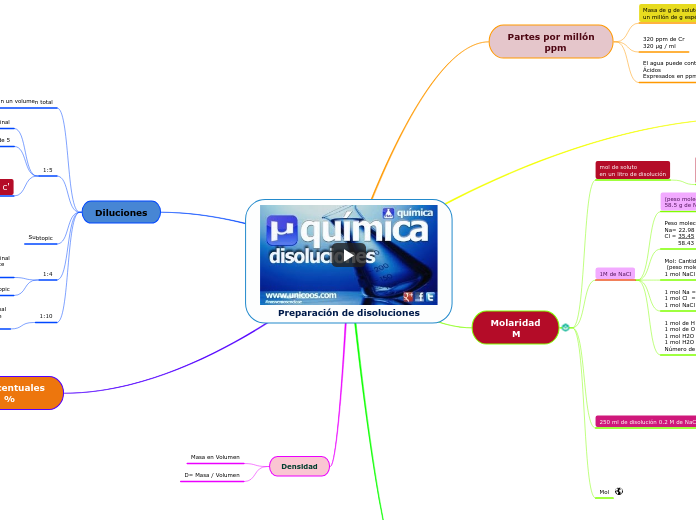
Preparación de disoluciones
da Hernández Pineda Hernández Pineda mancano 4 anni
417

Più simili a questo
20% Alcohol 20 ml de Alcohol 80 ml de solvente
40% 40 volúmenes en 100 volúmenes
5% 5g CuSO4 y 95g H2O
c' = concentración sol diluida
V' = Vol. sol. diluida
c = concentración
V= Volumen sol concentrada
Pesar 2,925 g NaCl Matraz aforado de 250 ml Agua hasta el aforo (enrase)