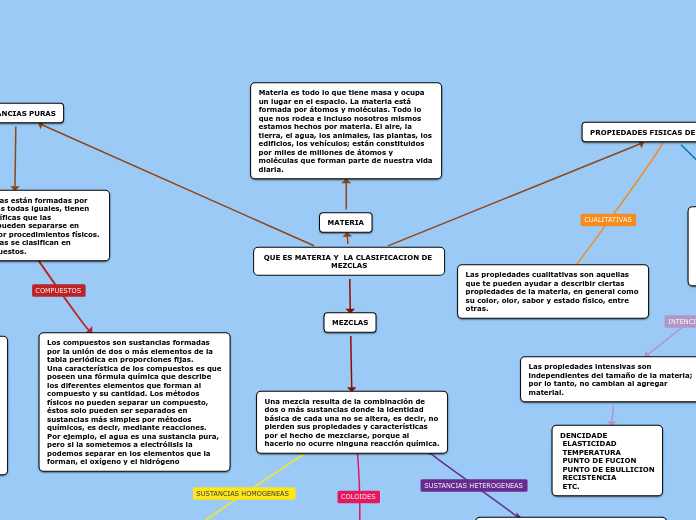
QUE ES MATERIA Y LA CLASIFICACION DE MEZCLAS
MEZCLAS
Una mezcla resulta de la combinación de dos o más sustancias donde la identidad básica de cada una no se altera, es decir, no pierden sus propiedades y características por el hecho de mezclarse, porque al hacerlo no ocurre ninguna reacción química.
Las mezclas heterogéneas presentan una composición no uniforme, sus componentes pueden distinguirse a simple vista, en otras palabras, se observan diferentes sustancias en la mezcla. Los componentes de este tipo de mezcla existen como regiones distintas que se llaman fases. Una mezcla heterogénea se compone de dos o más fases. Si observas la piedra de granito, puedes ver zonas de distinto color que indican que la roca está formada de cristales de distintas sustancias.
+Ensalada de lechuga y tomate
+Agua y arena
+Agua y aceite
+Helio y aire
+Aire y tierra
+Sopa con fideos
+Arroz y porotos
+Agua y azúcar
+Vinagre y aceite
+Salchichas con mayonesa
+Agua y nafta
+Papas y huevo
+Piedras y madera
+Agua y piedras
+Papeles y cintas
+Leche con malvaviscos
+Agua y parafina
+Galletas con dulce y manteca
+Papas fritas y maníes
+Madera y piedras
Las mezclas homogéneas se llaman también disoluciones. Tienen una apariencia totalmente uniforme por lo que sus componentes no pueden distinguirse a simple vista. Se dice que este tipo de mezclas tiene una sola fase. En química se denomina fase a una porción de materia con composición y propiedades uniformes. Por ejemplo, el agua de mar está formada por agua y muchas sales solubles, donde se observa una sola fase.
• Vino
• Preparación de torta
• Alpaca
• Café con leche
• OrO blanco
• Harina con azúcar glas
• Aire
• Agua con sal
• Mayonesa
• Masa de pizza
• Bronce
• Leche
• Jugo artificial
• Agua y alcohol
• Acero
• Gelatina
• Detergente y agua
• Cloro y agua
Se denomina como coloide a las mezclas de sustancias que se encuentra entre las soluciones y las suspensiones y cuyas partículas tienen un tamaño entre los 10 y 100 nanómetros.
-Crema de leche
-Leche
-Pinturas al látex
-Goma espuma
-Gelatina
-Niebla
-Humo
-Montmorillonita y demás arcillas silicatadas
-Materia orgánica
-Cartílago bovino
-Derivados de la albúmina
-Plasma
-Dextranos
-Hidroetilalmidones
-Tejido óseo
-Detergentes
-Sílica gel
-Óxido de titanio
MATERIA
Materia es todo lo que tiene masa y ocupa un lugar en el espacio. La materia está formada por átomos y moléculas. Todo lo que nos rodea e incluso nosotros mismos estamos hechos por materia. El aire, la tierra, el agua, los animales, las plantas, los edificios, los vehículos; están constituidos por miles de millones de átomos y moléculas que forman parte de nuestra vida diaria.
SUSTANCIAS PURAS
Las sustancias puras están formadas por átomos o moléculas todas iguales, tienen propiedades específicas que las caracterizan y no pueden separarse en otras sustancias por procedimientos físicos. Las sustancias puras se clasifican en elementos y compuestos.
Los elementos también pueden llamarse sustancias puras simples y están formados por una sola clase de átomos, es decir, átomos con el mismo número de protones en su núcleo y por lo tanto con las mismas propiedades químicas. Los elementos no pueden descomponerse en otras sustancias puras más sencillas por ningún procedimiento. Son sustancias puras simples todos los elementos químicos de la tabla periódica. A las sustancias formadas por moléculas compuestas por átomos iguales también se les considera elementos, por ejemplo el oxígeno gaseoso, oxígeno molecular o dioxígeno.
Los compuestos son sustancias formadas por la unión de dos o más elementos de la tabla periódica en proporciones fijas.
Una característica de los compuestos es que poseen una fórmula química que describe los diferentes elementos que forman al compuesto y su cantidad. Los métodos físicos no pueden separar un compuesto, éstos solo pueden ser separados en sustancias más simples por métodos químicos, es decir, mediante reacciones.
Por ejemplo, el agua es una sustancia pura, pero si la sometemos a electrólisis la podemos separar en los elementos que la forman, el oxígeno y el hidrógeno
PROPIEDADES FISICAS DE LA MATERIA
Las propiedades físicas de la materia son las características visibles y propias de una sustancia que pueden ser medidas y no producen nuevas sustancias químicas. Algunas de las propiedades físicas que podemos encontrar son, por ejemplo: Estado físico: sólido líquido, gaseoso o plasma (estados de la materia)
Las propiedades intensivas son independientes del tamaño de la materia; por lo tanto, no cambian al agregar material.
DENCIDADE
ELASTICIDAD
TEMPERATURA
PUNTO DE FUCION
PUNTO DE EBULLICION
RECISTENCIA
ETC.
Las propiedades extensivas son aquellas que dependen del tamaño o de la porción de la materia que se está considerando.
LONGUITUD
MASA
VOLUMEN
NUMERO DE MOLECULAS
RESISTENCIAS
CARGA ELECTRICA
ETC.
Las propiedades cualitativas son aquellas que te pueden ayudar a describir ciertas propiedades de la materia, en general como su color, olor, sabor y estado físico, entre otras.