によって Dario Franco Pineda Bermudez 4年前.
2370
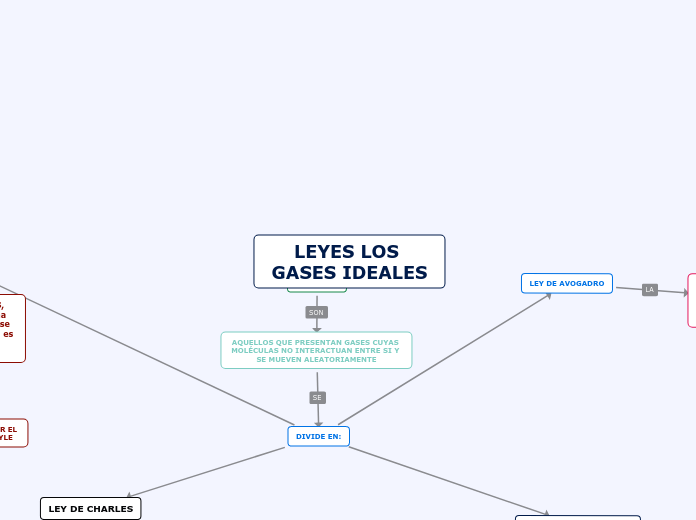
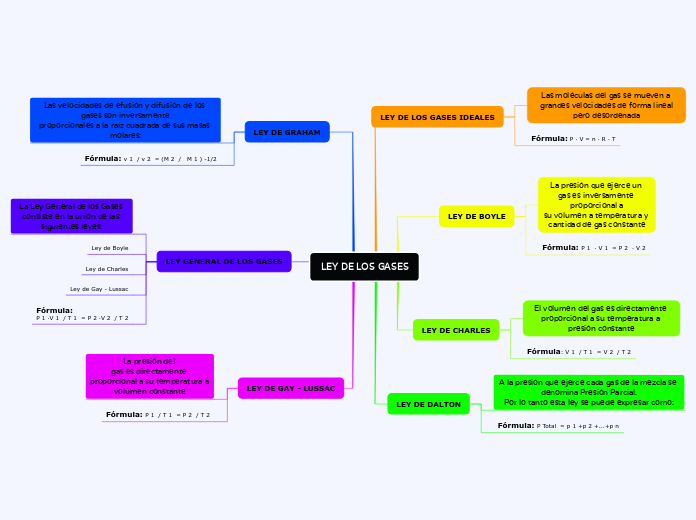
LEYES LOS GASES IDEALES
La comprensión del comportamiento de los gases ideales se basa en varias leyes fundamentales que describen cómo el volumen, la presión y la temperatura interactúan en diferentes condiciones.