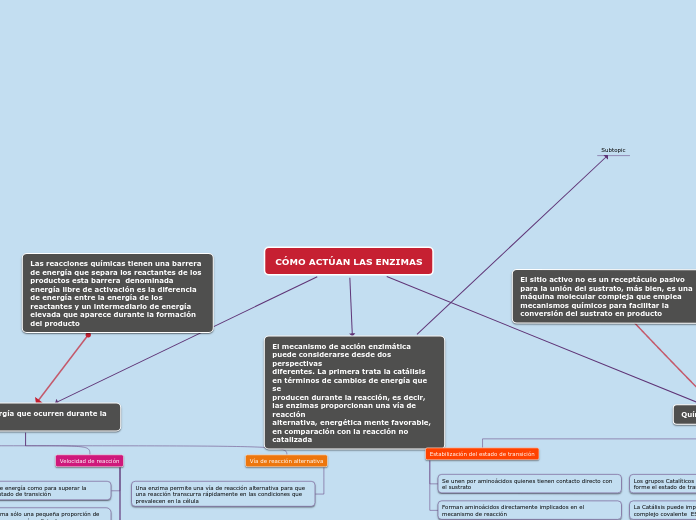
CÓMO ACTÚAN LAS ENZIMAS
cambios de energía que ocurren durante la reacción
Energía libre de activación
Velocidades de la reacción química no catalizadas suelen ser lentas
Velocidad de reacción
deben contener suficiente energía como para superar la barrera de energía del estado de transición
La ausencia de una enzima sólo una pequeña proporción de moléculas puede poseer esa energía suficiente como para alcanzar el estado de transición entre el reactante y el producto.
Vienen determinada por el numero de moléculas energizada
En general, cuanto menor sea la energía libre de activación mayor es el número de moléculas con energía suficiente para atravesar el estado de transición
Vía de reacción alternativa
Una enzima permite una vía de reacción alternativa para que una reacción transcurra rápidamente en las condiciones que prevalecen en la célula
El mecanismo de acción enzimática puede considerarse desde dos perspectivas
diferentes. La primera trata la catálisis en términos de cambios de energía que se
producen durante la reacción, es decir, las enzimas proporcionan una vía de reacción
alternativa, energética mente favorable, en comparación con la reacción no catalizada
Subtopic
Química del sitio activo
Estabilización del estado de transición
Se unen por aminoácidos quienes tienen contacto directo con el sustrato
Forman aminoácidos directamente implicados en el mecanismo de reacción
Otros mecanismos
Los grupos Catalíticos intensifican la probabilidad de que se forme el estado de transición.
La Catálisis puede implicar la formación transitoria de un complejo covalente ES
Visualización del estado de transición
La enzima se contacta formando así el ES análoga al estado de transición ES. esta conformación facilita la representación del grupo