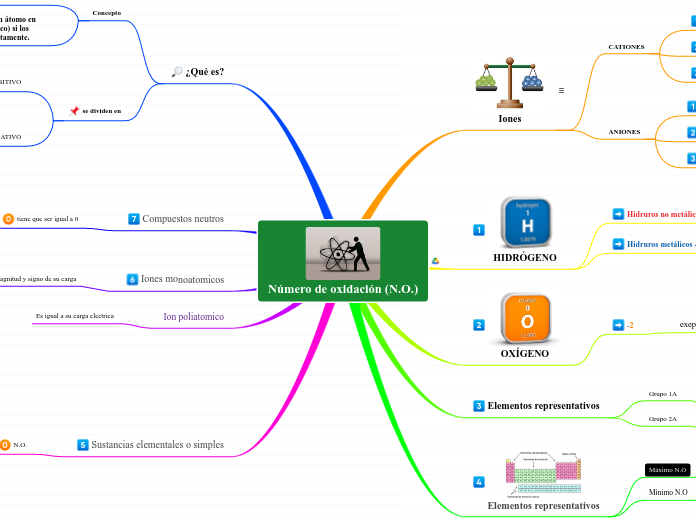
Número de oxidación (N.O.)

Iones
CATIONES
Na1+
Fe2+
Fe3+
ANIONES
Cl1-
S2-
N3-

HIDRÓGENO
Hidruros no metálicos +1
Ej. HF (ácido fluorhídrico)
Hidruros metálicos -1
Ej. NaH (hidruro de sodio)

OXÍGENO
-2
exepto
PEROXÍDOS -1
Elementos representativos
Grupo 1A
1+
Grupo 2A
2+

Elementos representativos
Máximo N.O
Igual al número de grupo (excepto O, F, Po)
Mínimo N.O
Se resta 8 al número de grupo
¿Qué es?
Concepto
Es la carga real o aparente que adquiere un átomo en un compuesto químico.
Es el número de cargas que tendría un átomo en
una molécula (o en un compuesto iónico) si los electrones fueran transferidos completamente.
se dividen en
POSITIVO
Si el elemento es un METAL
Si el elemento se combina con un átomo más electronegativo
NEGATIVO
si el elemento es un NO METAL
Si el elemento se combina con un átomo menos electronegativo
Compuestos neutros
tiene que ser igual a 0

Subtopic
Iones monoatomicos
Igual magnitud y signo de su carga
Ion poliatomico
Es igual a su carga electrica
Sustancias elementales o simples
N.O.