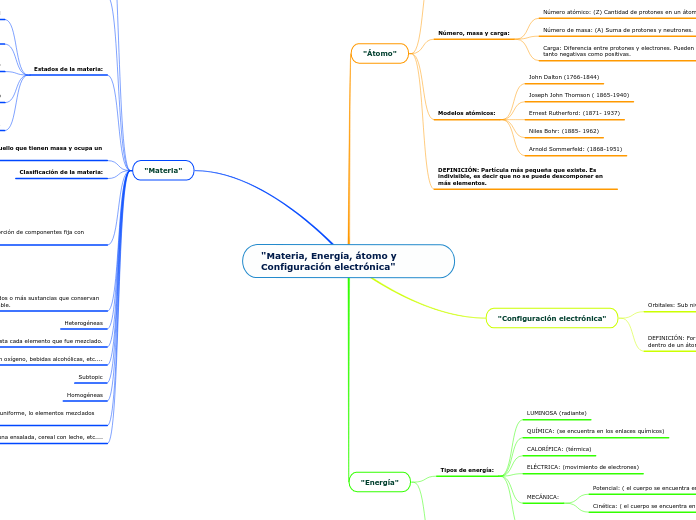
"Materia, Energía, átomo y Configuración electrónica"
"Átomo"
Estructura del átomo:
Protones: Partículas encontradas en el núcleo del átomo. Son positivas e identifican al átomo.
Electrones: Partículas encontradas alrededor del núcleo del átomo. Son negativas y su masa es más pequeña que la de los protones.
Neutrones: Partículas encontradas en la mayor parte del átomo. No tienen ninguna carga.
Número, masa y carga:
Número atómico: (Z) Cantidad de protones en un átomo.
Número de masa: (A) Suma de protones y neutrones.
Carga: Diferencia entre protones y electrones. Pueden ser tanto negativas como positivas.
Modelos atómicos:
John Dalton (1766-1844)
Joseph John Thomson ( 1865-1940)
Ernest Rutherford: (1871- 1937)
Niles Bohr: (1885- 1962)
Arnold Sommerfeld: (1868-1951)
DEFINICIÓN: Partícula más pequeña que existe. Es indivisible, es decir que no se puede descomponer en más elementos.
"Configuración electrónica"
Orbitales: Sub niveles en donde los electrones se albergan.
2- S, 6-P, 10-D, 14-F
PRINCIPIO DE AFBAU: Regla de diagonales, los orbitales se van ordenando en dirección diagonal.
DEFINICIÓN: Forma en la que los electrones se organizan dentro de un átomo.
"Energía"
Tipos de energía:
LUMINOSA (radiante)
QUÍMICA: (se encuentra en los enlaces químicos)
CALORÍFICA: (térmica)
ELÉCTRICA: (movimiento de electrones)
MECÁNICA:
Potencial: ( el cuerpo se encuentra en reposo)
Cinética: ( el cuerpo se encuentra en movimiento)
NUCLEAR: (fusión del núcleo en un átomo)
DEFINICIÓN: Capacidad de la materia para realizar un trabajo.
"Materia"
Cambios de estado:

DE LÍQUIDO A GASEOSO: Evaporación
DE LÍQUIDO A SÓLIDO: Solidificación
DE GASEOSO A LÍQUIDO: Condensación
DE GASEOSO A SÓLIDO: Cristalización
DE SÓLIDO A LÍQUIDO: Fusión
DE SÓLIDO A GASEOSO: Sublimación
Estados de la materia:
Condensado de Bose - EINSTEIN
No hay señal de ningún movimiento en absoluto. La matera es condensada llamada así un "súper átomo".
GASEOSO
Las partículas se mueven con absoluta libertad. Su volumen y forma son variables, también pueden ser comprimidos.
SÓLIDO
En el estado sólido, las partículas tienen una cantidad mínima de movimiento y permaneces unidas. Su forma y el volumen que tienen son fijos.
LÍQUIDO
El estado líquido permite a las partículas tener una gran libertad de movimiento, igualmente siguen unidas. Tienen un volumen fijo y una forma que varía.
PLASMA
Formado en presiones altas . Los electrones se escapan de los núcleos atómicos positivos.
DEFINICIÓN: "Todo aquello que tienen masa y ocupa un lugar en el espacio."
La materia no se puede crear ni destruir, solo podemos transformarla.
Clasificación de la materia:
Sustancias puras: Proporción de componentes fija con propiedades específicas.
Compuestos
Unión de elementos que pueden descomponerse en los elementos que se usaron para su composición.
Sal de mesa, azúcar, refrescos, alcohol, ácido clorhídrico, etc...
Elementos
Sustancia que no se descompone en más sustancias en particular.
Oxígeno, Plata, Cobre, Oro, nitrógeno, entre otros.
Mezclas: Formación por dos o más sustancias que conservan su origen, puede ser variable.
Heterogéneas
Se distingen a simple vista cada elemento que fue mezclado.
Nitrógeno con oxígeno, bebidas alcohólicas, etc....
Subtopic
Homogéneas
Al tener una composición uniforme, lo elementos mezclados no pueden distinguirse.
Agua con arena, una ensalada, cereal con leche, etc....