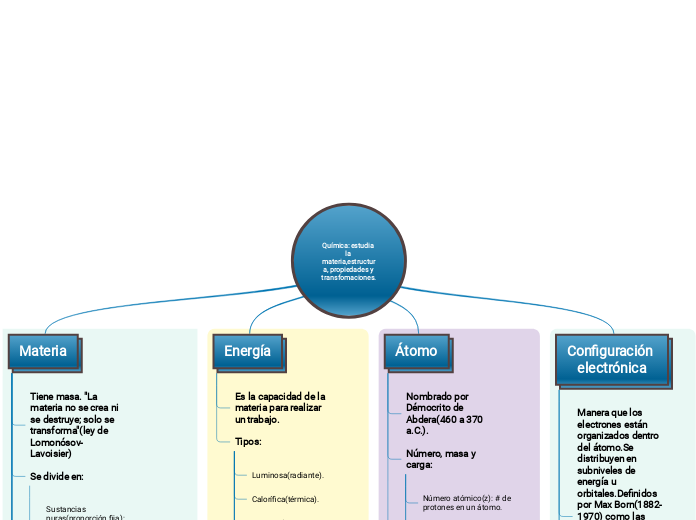
Química: estudia la materia,estructura, propiedades y transfomaciones.
.
Configuración electrónica
Regla de Hund: mismo tipo de orbital, los electrones no se aparean hasta que cada uno tiene un electrón. Aplica a partir de orbitales p.
Principio de aufbau o regla de las diagonales: los orbitales se van llenadno en orden ascendente de energía hasta llegar al total de electrones.
Manera que los electrones están organizados dentro del átomo.Se distribuyen en subniveles de energía u orbitales.Definidos por Max Born(1882-1970) como las regiones espaciales(nubes electrónicas) donde la probabilidad de encontrar un electrón es la máxima. Se utilizan 4 tipos: s, p, d y f.Máximo de electrones:
14 en f.
10 en d.
6 en p.
2 en s.
Átomo
Átomo, iones, isótopos:
Átomos del mismo elemento pueden tener diferente número de neutrones en el núcleo. A estos se les conoce como isótopos.
El átomo es neutro mismos protones y electrones.Puede ganar o perder electrones (de la órbita más externa y se conocen como electrones de enlace o de valencia)convirtiéndose en un ion y ser:
Negativo o anión( se ganan electrones).
Positivo o catión(se pierden electrones).
Número, masa y carga:
Carga: diferencia entre protones y electrones( puede ser positiva o negativa).
Número de masa(A): suma de protones y neutrones.
Número atómico(z): # de protones en un átomo.
Nombrado por Démocrito de Abdera(460 a 370 a.C.).
Energía
Tipos:
Nuclear( fisión/fusión del núcleo del átomo).
Mecánica:
Cinética:(por su movimiento).
Potencial(por la posición del cuerpo en reposo).
Eléctrica(movimiento de electrones)
Química(en los enlaces químicos).
Calorífica(térmica).
Luminosa(radiante).
Es la capacidad de la materia para realizar un trabajo.
Materia
Los cambios de estado son cambios de temperatura.
Estados de la materia:
Plasma: más común en el universo; poco frecuente en la tierra. Altas presiones y temperaturas. Los electrones"escapan" de los núcleos atómicos positivos.
Gas: prácticamente no hay fuerza de cohesión entre ellas. Volumen y forma variable, se puede comprimir.
Líquido: mayor libertad de movimiento, volumen fijo y forma variable.
Sólido: muy poco movimiento, volumen y forma fijos.
Condensado de Bose-Einsein: ausencia de movimiento.
Cambios de la materia:
Físicos: internamente intacto,cambia forma,tamaño,etc...
Químicos: transforman sustancias en otras(reacciones químicas)..
Propiedades de la materia:
Físicas:
Químicas: capacidad de una sustancia a transformarse en otra.
Extensivas o generales: dependen de la cantidad de esta.
Intensivas o específicas: independientes a cantidad de materia.
Las mezclas se separan por:
Filtración:mezclas heterogéneas sólido-líquido.
Destilación: mezclas homogéneas líquido-líquido.
Decantación: mezclas homogéneas líquido-líquido.
Evaporación: mezclas homogéneas sólido-líquido.
Se divide en:
Sustancias puras(proporción fija): Elementos(forma simple de la materia, no se descompone) y Compuestos(formados por 2 o más elementos.Pueden descomponerse) .
Mezclas( 2 o más sustancias puras.La proporción de sus componentes es variable): Homogéneas(composición uniforme, no se distinguen sustancias) y Heterogéneas(su composición varía y se distinguen las sustancias que la forman).
Tiene masa. "La materia no se crea ni se destruye; solo se transforma"(ley de Lomonósov-Lavoisier)