ESTADO GASEOSO

CONCEPTO
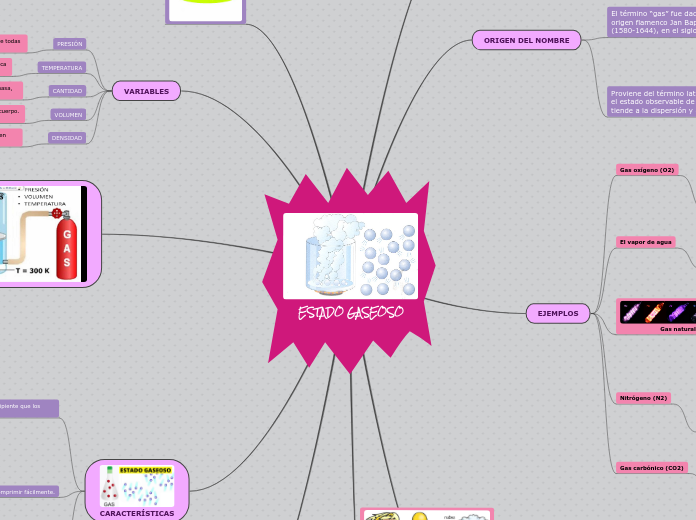
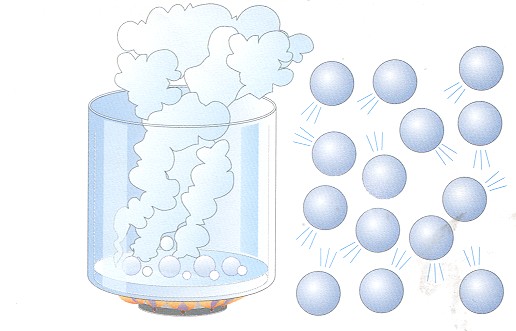
El estado gaseoso es el estado de agregación de la materia que carece de volumen y de forma propios, algo que le permite diferenciarse de un líquido o de un sólido.
ORIGEN DEL NOMBRE
El término “gas” fue dado por el científico de origen flamenco Jan Baptista van Helmont (1580-1644), en el siglo XVII.

Jan Baptista van Helmont
Proviene del término latino chaos (“caos”), pues el estado observable de las partículas de un gas tiende a la dispersión y a un aparente desorden.
EJEMPLOS
Gas oxígeno (O2)

El vapor de agua


Gas natural
neón
kriptón
radón
xenón
oganesón.
Nitrógeno (N2)

Gas carbónico (CO2)


Topic principal
Subtopic
VARIABLES
PRESIÓN
En los gases esta fuerza actúa en forma uniforme sobre todas las partes del recipiente.
760 mm de Hg = 1 atmósfera
TEMPERATURA
La temperatura de un gas es proporcional a la energía cinética media de las moléculas del gas.
K = °C + 273
CANTIDAD
La cantidad de un gas se puede medir en unidades de masa, usualmente en gramos
VOLUMEN
Es el espacio ocupado por un cuerpo.
Unidades de volumen:
m3 = 1 000 litros;
1 cm3 = 1 mL ; 1 L = 103 mL = 1 000 cm3
DENSIDAD
Es la relación que se establece entre la masa molecular en gramos de un gas y su volumen molar en litros
unidad: g/L

CARACTERÍSTICAS
Se adaptan a la forma y el volumen del recipiente que los contiene.

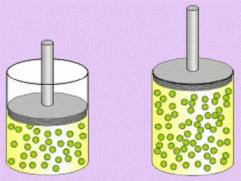
Se dejan comprimir fácilmente.
Al existir espacios intermoleculares, las moléculas se pueden acercar unas a otras reduciendo su volumen, cuando aplicamos una presión.
Se difunden fácilmente
Al no existir fuerza de atracción intermolecular entre sus partículas, los gases se esparcen en forma espontánea.