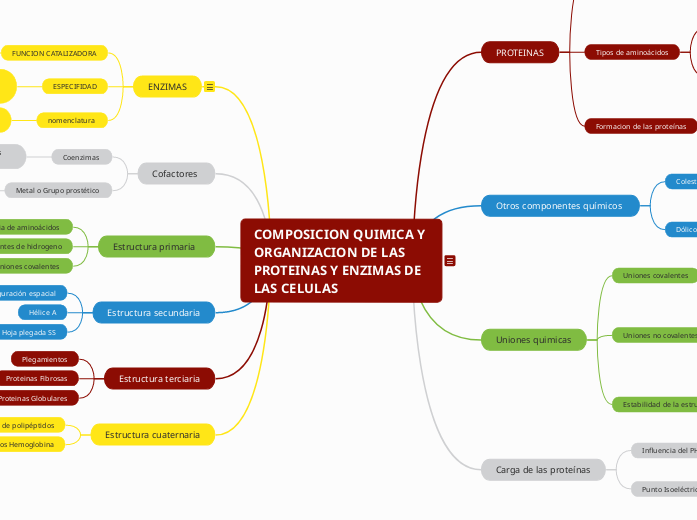
COMPOSICION QUIMICA Y ORGANIZACION DE LAS PROTEINAS Y ENZIMAS DE LAS CELULAS
ENZIMAS
FUNCION CATALIZADORA
Las enzeimas son las encargadas de la aceleración de las reacciones quimicas sin modificarse
ESPECIFIDAD
Las enzimas presentan una gran especifidad, ya que solo pueden actuar sobre un sustrato en particular
nomenclatura
Las enzimas son nombradas segun el sustrato el cual modifican o la actividad que realizen
Cofactores
Coenzimas
Ciertas enzimas necesitan la ayuda de coenzimas para poder llevar a cabo su función
Metal o Grupo prostético
En ciertas situaciones, el cofactor de una enzima puede ser un metal o un grupo prostético que se encuentra unido covalentemente a la proteína
Estructura primaria
Secuencia de aminoácidos
Puentes de hidrogeno
Uniones covalentes
Estructura secundaria
Configuración espacial
Hélice A
Hoja plegada SS
Estructura terciaria
Plegamientos
Proteinas Fibrosas
Proteinas Globulares
Estructura cuaternaria
combinación de polipéptidos
Ejemplos Hemoglobina
PROTEINAS
Estructura de los aminoácidos
Los aminoácidos son los monómeros que
componen las proteínas y están formados por un grupo carboxilo, un grupo amino y un residuo lateral.
Tipos de aminoácidos
AMINOÁCIDOS ÁCIDOS Y BÁSICOS
Los aminoácidos de tipo ácido poseen un grupo carboxilo extra en su cadena lateral, mientras que los aminoácidos básicos cuentan con un grupo amino adicional en esa misma región.
AMINOÁCIDOS NEUTROS POLARES Y NO POLARES
Los aminoácidos neutros con cadenas polares tienen afinidad por el agua (son hidrofílicos), mientras que aquellos con cadenas no polares tienden a evitarla (son hidrofóbicos).
Formacion de las proteínas
Las proteínas se generan mediante enlaces peptídicos que se establecen entre los grupos amino y carboxilo de los aminoácidos, dando lugar a una cadena de tipo proteico.
Otros componentes químicos
Colesterol
El colesterol es un compuesto orgánico, una sustancia grasa, que se encuentra en las membranas celulares y se deriva de
un compuesto de 17 carbonos.
Dólicol y ubiquinona
El dolicol y la ubiquinona son moléculas compuestas por unidades de isopreno y desempeñan funciones esenciales dentro de las células.
Uniones quimicas
Uniones covalentes
Las uniones covalentes surgen cuando un par de átomos comparte electrones entre sí.
Uniones no covalentes
Puentes de Hidrogeno
Los enlaces de hidrógeno son interacciones débiles que se establecen entre un átomo de hidrógeno y otro átomo con alta electronegatividad.
Fuerza FisicoQuímica
Las fuerzas físicoquímicas son las responsables de la disociación de las uniones no covalentes.
La estabilidad de la estructura molecular .
Estabilidad de la estructura molecular
La presencia de múltiples interacciones no covalentes dentro de una molécula ayuda a mantener su estabilidad estructural.
Carga de las proteínas
Influencia del PH
El pH influye en la carga de las proteínas, ya que modifica la disociación de sus grupos ácidos y básicos.
Punto Isoeléctrico
El punto isoeléctrico corresponde al valor de pH en el que una proteína no presenta carga neta, es decir, su carga total es neutra.