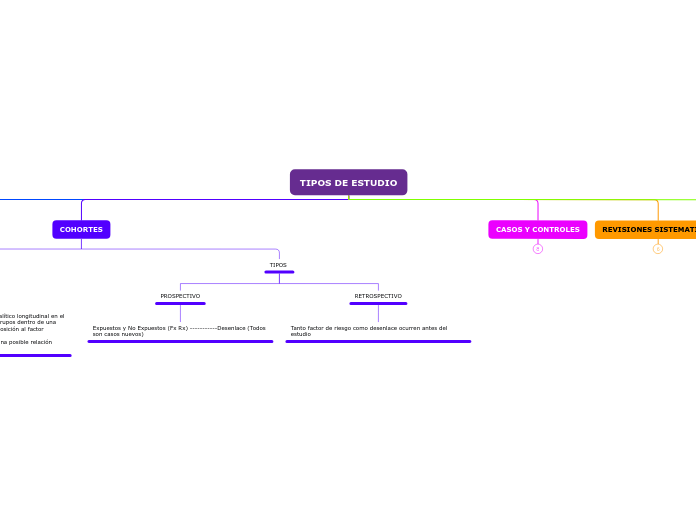
TIPOS DE ESTUDIO
ENSAYO CLINICO ALEATORIZADO
EL INVESTIGADOR CONTROLA EL FACTOR DE ESTUDIO
QUE CONTROLA
SUJETOS
INTERVENCION
FORMA (Dosis, duración)
OBJETIVO
EVALUAR EFECTO
ANALÍTICOS - PROSPECTIVOS
MUESTRA (Posterior a exclusiones o rechazos)
Asignación Aleatoria (Asegurar la comparabilidad de los grupos, de manera que la comparación
entre las intervenciones o tratamientos sea lo más
imparcial posible, tiende a producir una distribución equilibrada de las variables entre los grupos, tanto de las conocidas como de las que no lo son) y permite
la utilización de técnicas de ENMASCARAMIENTO, que
son muy útiles para obtener una estimación no sesgada de la variable de respuesta.
Grupo A
Intervención de Estudio
Grupo B
Intervención de Comparación (Placebo
COHORTES
El término cohorte se utiliza para designar a un grupo
de sujetos que tienen una característica o un conjunto de características en común (generalmente la exposición al factor de estudio),
1 COHORTE: Cuando solamente existe una
cohorte que es seguida en el tiempo / incidencia o evolución, se trata de un diseño descriptivo longitudinal
2 COHORTES: Diseño observacional analítico longitudinal en el que se comparan dos cohortes, o dos grupos dentro de una misma cohorte, que difieren por su exposición al factor
de estudio, con el objetivo de evaluar una posible relación causa-efecto
TIPOS
PROSPECTIVO
Expuestos y No Expuestos (Fx Rx) -----------Desenlace (Todos son casos nuevos)
RETROSPECTIVO
Tanto factor de riesgo como desenlace ocurren antes del estudio
CASOS Y CONTROLES
REVISIONES SISTEMATICAS
OTROS DISEÑOS EXPERIMENTALES
Desarrollo clínico
de medicamentos
Investigación PreClinica
Durante la cual se realizan estudios de laboratorio y en animales para demostrar la actividad biológica del compuesto en una determinada enfermedad y evaluar su seguridad. / 3 años y medio
Desarrollo
Clínico
Pequeña escala / Seguridad / 1 año /Sujetos voluntarios sanos
Mayor escala / Eficacia Terapéutica / 100 a 300 voluntarios / 2 años
Fase de la evaluación de un medicamento antes de su comercialización
Evaluar la eficacia y relación beneficio/riesgo en comparación con otras alternativas terapéuticas disponibles, o con un placebo si no hay tratamiento disponible. Permite establecer la eficacia del nuevo fármaco e identificar y cuantificar los efectos indeseables más frecuentes. /1.000 a 3.000 individuos /3 años / Ensayos clínicos aleatorios
OTROS
Métodos Secuenciales. Se trata de ensayos en los que el tamaño de la muestra no está predeterminado, sino que
depende de las observaciones que se realizan. Su característica principal es la definición de una regla de
finalización explícita en la que se establece la forma
en que la decisión de finalizar el estudio depende
de los resultados obtenidos hasta ese momento
Evaluación de tratamientos
no farmacológicos: Aproximadamente el 25% de los ensayos clínicos que se publican evalúan intervenciones no farmacológicas, como la cirugía, la rehabilitación, la psicoterapia, las terapias conductuales o las terapias alternativas.
Evaluación de la eficacia
de medidas preventivas. / Evaluación de la eficacia
de pruebas diagnósticas
Ensayo clínico factorial / Ensayo clínico cruzado / Ensayos comunitarios
Ensayos controlados no aleatorios / Ensayos no controlados
Subtopic