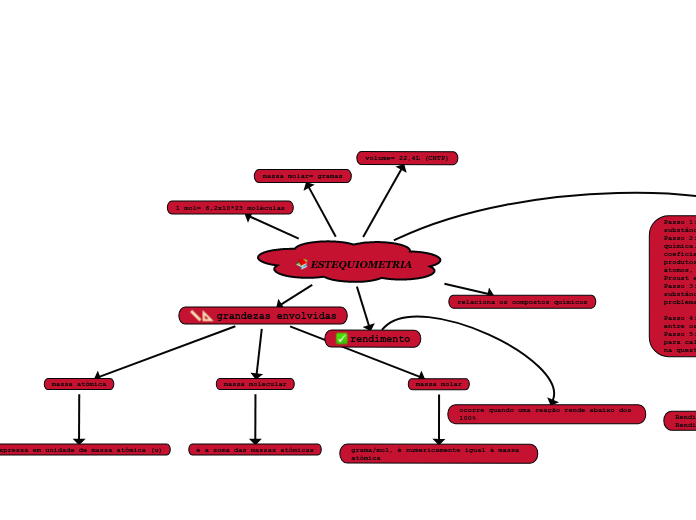
ESTEQUIOMETRIA
grandezas envolvidas
massa atômica
expressa em unidade de massa atômica (u)
massa molecular
é a soma das massas atômicas
massa molar
grama/mol, é numericamente igual á massa atômica
relaciona os compostos químicos
rendimento
ocorre quando uma reação rende abaixo dos 100%
Passo 1: Escreva a equação química com as substâncias envolvidas;
Passo 2: Faça o balanceamento da equação química. Para isso, é preciso ajustar os coeficientes para que reagentes e produtos contenham a mesma quantidade de átomos, segundo as Leis Ponderais (Lei de Proust e Lei de Lavoisier);
Passo 3: Escreva os valores das substâncias, seguindo os dados do problema e identificando o que se pede;
Passo 4: Estabeleça a relação existente entre os números de moles, massa, volume. Passo 5: Faça uma regra de três simples para calcular os valores que são pedidos na questão ou problema.
Rendimento teórico ----------- 100 %
Rendimento real -------------- X