sales halogenas
neutras
Se dan por la reacción entre: un ácido hidrácido o compuesto especial + hidróxido. No se simplifican, Siempre liberan agua. 4.
ejemplos
NaCl: Cloruro de sodio
CaCl2: Cloruro de calcio
CaSO4: Sulfato de calcio
KNO3: Nitrato de potasio
CaF2: Fluoruro de calcio
hidracidos
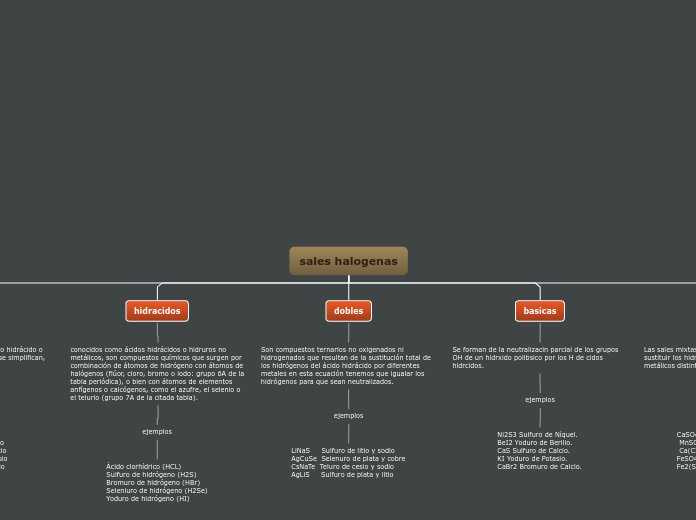
conocidos como ácidos hidrácidos o hidruros no metálicos, son compuestos químicos que surgen por combinación de átomos de hidrógeno con átomos de halógenos (flúor, cloro, bromo o iodo: grupo 6A de la tabla periódica), o bien con átomos de elementos anfígenos o calcógenos, como el azufre, el selenio o el telurio (grupo 7A de la citada tabla).
ejemplos
Ácido clorhídrico (HCL)
Sulfuro de hidrógeno (H2S)
Bromuro de hidrógeno (HBr)
Seleniuro de hidrógeno (H2Se)
Yoduro de hidrógeno (HI)
dobles
Son compuestos ternarios no oxigenados ni hidrogenados que resultan de la sustitución total de los hidrógenos del ácido hidrácido por diferentes metales en esta ecuación tenemos que igualar los hidrógenos para que sean neutralizados.
ejemplos
LiNaS Sulfuro de litio y sodio
AgCuSe Selenuro de plata y cobre
CsNaTe Teluro de cesio y sodio
AgLiS Sulfuro de plata y litio
basicas
Se forman de la neutralizacin parcial de los grupos OH de un hidrxido polibsico por los H de cidos hidrcidos.
ejemplos
Ni2S3 Sulfuro de Níquel.
BeI2 Yoduro de Berilio.
CaS Sulfuro de Calcio.
KI Yoduro de Potasio.
CaBr2 Bromuro de Calcio.
mixtas
Las sales mixtas son compuestos, resultado de sustituir los hidrógenos de un ácido por átomos metálicos distintos de hidróxidos.
ejemplos
CaSO4 = Sulfato de calcio.
MnSO3 = Sulfito de manganeso.
Ca(CIO2)2 = Clorito de calcio.
FeSO4 = Sulfato ferroso.
Fe2(SO4)3 = Sulfato férrico.