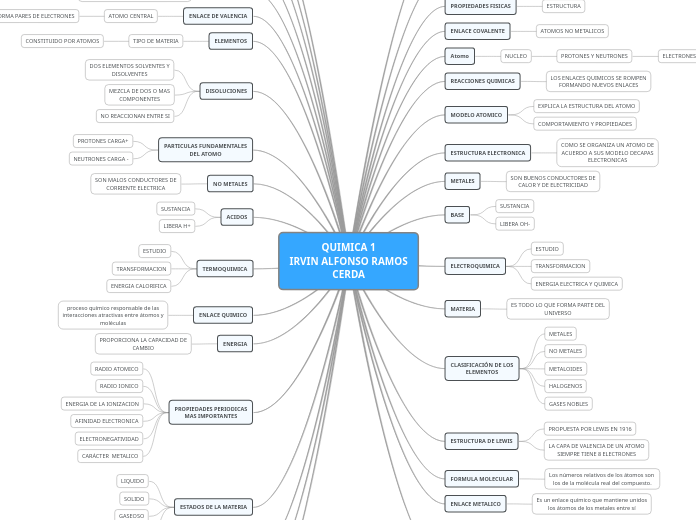
QUIMICA 1
IRVIN ALFONSO RAMOS
CERDA
CIENCIA
QUE ESTUDIA
LA MATERIA
QUIMICA ORGANICA
ESTUDIA
COMPUESTOS DE TIPO ORGANICO
PROPIEDADES FISICAS
ESTRUCTURA
ENLACE COVALENTE
ATOMOS NO METALICOS
Atomo
NUCLEO
PROTONES Y NEUTRONES
ELECTRONES
REACCIONES QUIMICAS
LOS ENLACES QUIMICOS SE ROMPEN
FORMANDO NUEVOS ENLACES
MODELO ATOMICO
EXPLICA LA ESTRUCTURA DEL ATOMO
COMPORTAMIENTO Y PROPIEDADES
ESTRUCTURA ELECTRONICA
COMO SE ORGANIZA UN ATOMO DE
ACUERDO A SUS MODELO DECAPAS
ELECTRONICAS
METALES
SON BUENOS CONDUCTORES DE
CALOR Y DE ELECTRICIDAD
BASE
SUSTANCIA
LIBERA OH-
ELECTROQUIMICA
ESTUDIO
TRANSFORMACION
ENERGIA ELECTRICA Y QUIMICA
MATERIA
ES TODO LO QUE FORMA PARTE DEL
UNIVERSO
CLASIFICACIÓN DE LOS
ELEMENTOS
METALES
NO METALES
METALOIDES
HALOGENOS
GASES NOBLES
ESTRUCTURA DE LEWIS
PROPUESTA POR LEWIS EN 1916
LA CAPA DE VALENCIA DE UN ATOMO
SIEMPRE TIENE 8 ELECTRONES
FORMULA MOLECULAR
Los números relativos de los átomos son
los de la molécula real del compuesto.
ENLACE METALICO
Es un enlace químico que mantiene unidos
los átomos de los metales entre sí
ORBITALES
se ordenan los orbitales en base a su nivel
energético creciente
En un átomo los electrones ocuparán
orbitales de forma que su energía sea la
menor posible.
La energía de los orbitales para átomos de
varios electrones viene determinada por
los números cuánticos n y l.
TABLA PERIODICA
CLASIFICACION
DE LOS ELEMENTOS
COMPUESTOS QUIMICOS
OXIDOS
HIDROXIDOS
ES LA UNIÓN DE 2 O MAS ELEMENTOS
COMPUESTOS
ENLACES
FUERZAS QUE MANTIENE UNIDOS A LOS
ATOMOS
ENLACE DE VALENCIA
ATOMO CENTRAL
FORMA PARES DE ELECTRONES
ELEMENTOS
TIPO DE MATERIA
CONSTITUIDO POR ATOMOS
DISOLUCIONES
DOS ELEMENTOS SOLVENTES Y
DISOLVENTES
MEZCLA DE DOS O MAS
COMPONENTES
NO REACCIONAN ENTRE SI
PARTICULAS FUNDAMENTALES
DEL ATOMO
PROTONES CARGA+
NEUTRONES CARGA -
NO METALES
SON MALOS CONDUCTORES DE
CORRIENTE ELECTRICA
ACIDOS
SUSTANCIA
LIBERA H+
TERMOQUIMICA
ESTUDIO
TRANSFORMACION
ENERGIA CALORIFICA
ENLACE QUIMICO
proceso químico responsable de las
interacciones atractivas entre átomos y
moléculas
ENERGIA
PROPORCIONA LA CAPACIDAD DE
CAMBIO
PROPIEDADES PERIODICAS
MAS IMPORTANTES
RADIO ATOMICO
RADIO IONICO
ENERGIA DE LA IONIZACION
AFINIDAD ELECTRONICA
ELECTRONEGATIVIDAD
CARÁCTER METALICO
ESTADOS DE LA MATERIA
LIQUIDO
SOLIDO
GASEOSO
PLASMA
FORMULA ESTRUCTURAL
Indica cómo están enlazados los átomos
en la molécula.
MODELO DE BOHR
Bohr propuso para el átomo de hidrógeno,
un núcleo formado por una partícula
positiva, y girando alrededor de ella, un
electrón
HIDROCARBUROS
son un grupo de compuestos orgánicos
que contienen principalmente carbono e
hidrógeno