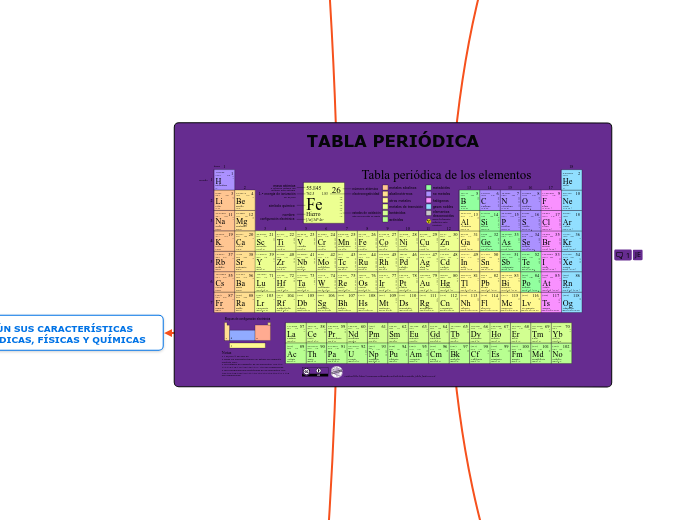
TABLA PERIÓDICA
LINEA DEL TIEMPO
DE LA TABLA PERIODICA
SEGÚN
GRUPOS, FAMILIAS Y PERIODOS
GRUPOS
GRUPO A
Grupo 1 (I A):
Los metales alcalinos
Grupo 2 (II A):
Los metales Alcalinotérreos
Grupo 13 (III A):
Familia del Boro
Grupo 14 (IV A):
Familia del Carbono
Grupo 15 (V A):
Familia del Nitrógeno
Grupo 16 (VI A):
Familia del Oxigeno
Grupo 17 (VII A):
Halógenos
Grupo 18 (VIII A):
Gases nobles
GRUPO B
Grupo 3 (III B):
Familia del Escandio (tierras raras y actinidos)
Grupo 4 (IV B):
Familia del Titanio
Grupo 5 (V B):
Familia del Vanadio
Grupo 6 (VI B):
Familia del Cromo
Grupo 7 (VII B):
Familia del Manganeso
Grupo 8 (VIII B):
Familia del hierro
Grupo 9 (VIII B):
Familia del Cobalto
Grupo 10 (VIII B):
Familia del Níquel
Grupo 11 (I B):
Familia del Cobre
Grupo 12 (II B):
Familia del Zinc
FAMILIAS
Familia de Metales Alcalinos:
Grupo 1 (I A)
Familia de los Metales Alcalinotérreos:
Grupo 2 (II A)
Familia de los Metales de transición:
Grupos del 3 al 12 ( I B al VIII B)
Familia del Boro o Térreos:
Grupo 13 (III A)
Familia del Carbono o Carbonoides:
Grupo 14 (IV A)
Familia del Nitrógeno o Nitrogenoides:
Grupo 15 (V A)
Familia del Oxígeno o Calcógenos:
Grupo 16 (VIA)
Familia de los Halógenos:
Grupo 17 (VIIA)
Familia de los Gases Nobles:
Grupo 18 (VIIIa)
Otros Metales
PERIODOS
PRIMER PERIODO
2 Elementos
SEGUNDO PERIODO
8 Elementos
TERCER PERIODO
8 Elementos
CUARTO PERIODO
18 Elementos
QUINTO PERIODO
18 Elementos
SEXTO PERIODO
32 Elementos
SEPTIMO PERIODO
32 Elementos
INFORMACIÓN DE
CADA UNO DE SUS ELEMENTOS
PUNTO DE EBULLICIÓN
El punto de ebullición varía de un elemento a otro
DEPENDE DE FACTORES COMO:
La masa molecular
La geometría molecular
NÚMERO ATÓMICO
PESO ATÓMICO
PUNTO DE FUSIÓN
DEPENDE DE FACTORES COMO:
La fuerza de los enlaces interatómicos
La masa atómica
La estructura cristalina del sólido
ESTRUCTURA ATÓMICA
SIMBOLO DE UN ELEMENTO
EN
INGLÉS
LATÍN
GRIEGO
DENSIDAD
La densidad se expresa
NOMBRE
Cada elemento tiene un nombre único que lo identifica dentro de la tabla periódica de los elementos.
El nombre de un elemento puede estar relacionado
CON
SU DESCUBRIMIENTO
SUS PROPIEDADES FÍSICAS O QUÍMICAS
SU ORIGEN
SU USO
SEGÚN SUS CARACTERÍSTICAS
PERÍODICAS, FÍSICAS Y QUÍMICAS
BLOQUE "S"
BLOQUE "P"
BLOQUE "D"
BLOQUE "F"
SEGÚN CARACTERÍSTICAS FÍSICAS
Metales
ALCALINOS
ALCALINOTÉRREOS
METALES DE
TRANSICIÓN / BLOQUE D
LANTÁNIDOS / ACTÍNIDOS
OTROS METALES
Metaloides
No Metales
OTROS NO METALES
HALÓGENOS
GASES NOBLES
SEGÚN SUS CARACTERÍSTICAS QUÍMICAS
Elementos Representativos
Metales de Transición
Elementos de Transición interna
Gases Nobles
SEGÚN
PROPIEDADES PERIÓDICAS DE LOS ELEMENTOS
RADIO ATÓMICO
RADIO ATÓMICO
ASIGNA A CADA ELEMENTO UN RADIO ATOMICO APROXIMADO LA MITAD DE LA DISTANCIA ENTRE LOS NUCLEOS DE LOS ATOMOS.
VARIA
RADIO IÓNICO (RI)
RADIO IÓNICO
ES CUANDO UN ATOMO SE IONIZA
MODIFICA SU VOLUMEN
SI
PIERDE ELECTRONES
SE CONVIERTE EN ANIÓN
POR LO TANTO
GANA ELECTRONES
SE CONVIERTE EN CATIÓN
POR LO TANTO
ENERGÍA DE IONIZACIÓN
ENERGÍA DE IONIZACIÓN
VARIA
AFINIDAD ELECTRÓNICA
AFINIDAD ELECTRÓNICA
VARIA
ELECTRONEGATIVIDAD
ELECTRONEGATIVIDAD
ELECTRONEGATIVIDAD ALTA
TIENEN UNA GRAN CAPACIDAD PARA ATRAER ELECTRONES
ELECTRONEGATIVIDAD BAJA
TIENEN MENOS CAPACIDAD PARA ATRAER ELECTRONES