по Diego Gutierrez 2 лет назад
184
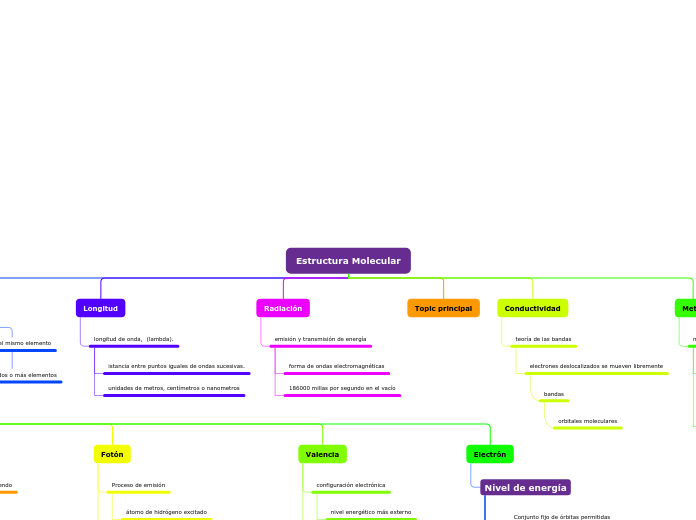
Estructura Molecular
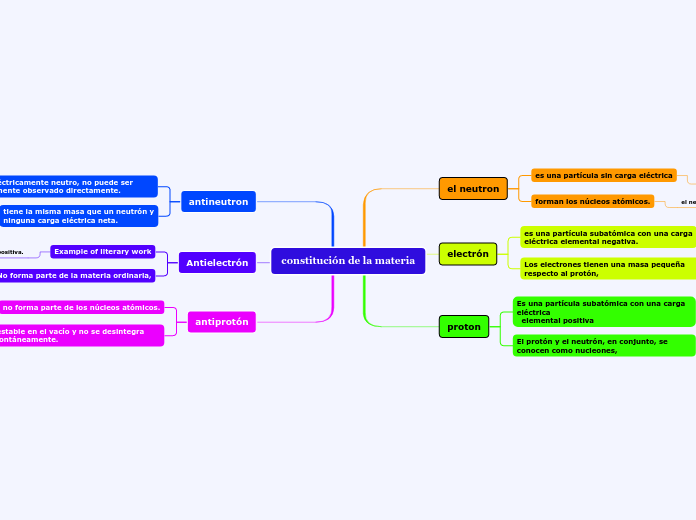
En la química y la física, los conceptos fundamentales como el átomo y el electrón juegan roles cruciales en la comprensión de las propiedades y comportamientos de la materia. La teoría atómica de Dalton describe al átomo como una partícula extremadamente pequeña e indivisible, siendo la unidad básica de un elemento.