по isabelle butinholi 3 лет назад
152
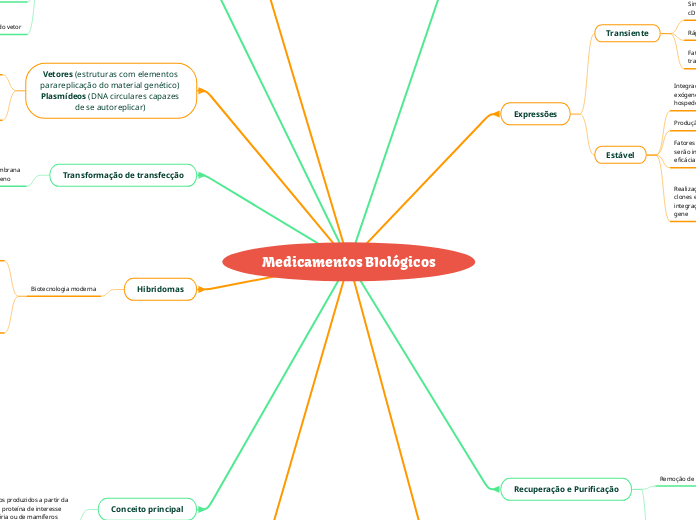
Medicamentos BIológicos
по isabelle butinholi 3 лет назад
152

Больше похоже на это
PCR
Uso de transcriptase reversa para produção do cDNA a partir do DNA
Partir do RNAm pois o DNA possui íntrons e éxons - retirados no processamento de RNA
Primers específicos para a sequência de interesse
Custo de produção
Velocidade de replicação da célula
Padrão de modificação pós taducional (em especial glicosilação)
LINHAGEM RECOMBINANTE
Inserção do gene de interesse em um vetor para carrear o fragmento até o genoma da célula hospedeira
Utilizando enzimas de restrição - 2 gerar extremidade coesivas (utilizar as mesmas enzimas no gene e no plasmídeo)
Permite o desenvolvimento de moléculas mais eficientes - maior tempo de meia vida, maior efetividade
Produção em larga escala e com alta qualidade final (pureza)
Sequência de resíduos de aminoácidos idêntica a da proteína humana - maior compatibilidade com o organismo humano
Também relacionados com a alta complexidade das moléculas, tornando o processo custoso e caro - Heterogenicidade nas macromoléculas
Principalmente relacionado à imonogenicidade desses medicamentos e risco de contaminação, principalmente por vírus
Exemplos:
Tratuzumabe - anticorpo monoclonal usado no tratamento do cancer. Bloqueia a sinalização intracelular inibindo a ploriferação de células tumorais
Natalizumabe é indicado como terapia única no tratamento da Esclerose Múltipla recorrente-remitente, para prevenir surtos e retardar a progressão da doença
Adalimumabe: destinado ao tratamento da artrite reumatoide grave, ativa e progressiva em pacientes.Anticorpo monoclonal humano Anti-TNF alfa
Utilização de:
Célula mieloma (replicação ilimitada)
Células esplênicas com anticorpos desejado (replicação limitada)
fusão das células
Formam o hibridoma com capacidade de multiplicação indefinida e pode produzir o Ac monoclonal que se deseja
Cultivo emmeio adequado
Propagação
Processo ocorre em fermentadores ou em céluas animais (in vivo)
Permitem o crescimento apenas dos hibridomas
Seleção da célula que produz o anticorpo de interesse
Isolamento de uma única célula que produzirá um único tipo de anticorpo
Interagem com o mesmo epítopo
Possuem a mesma região de complementariedade ( região variável)
Derivados de uma mesma linhagem
Aumento repentino de temperatura criando diferenças de pressão entre o exterior e o interior da célula induzindo a formação de poros na membrana
Campo eléctrico é aplicado nas células de modo a aumentar a permeabilidade da membrana celular
Etapa 1- Clarificação:separação das células do meiode cultivo (por filtração ou centrifugação)
Etapa final - Polimento
Remoção de contaminantes que são mais parecidos com a proteína de interesse
Uso de cromatografia de exclusão molecular ou troca iônica
Diafiltração final ocorre nessa etapa
Etapa intercalada- Diafiltração (caso seja necessário) - processo de troca do solvente utilizado
Diafiltraçãp final - colocar a proteína purificada em um tampão com pH adequado para o envase e administração
Uso de poros muito pequenos que retem a nossa proteína de interesse - ocorre também o aumento da concentração da proteína
Etapa 2- Recuperação / isolamento primário
Filtração esterilizante - reduzir os riscos de contaminação viral
nanofitração associado a métodos químicos de remoção (detergente,pH ácido)
Cromatografia Líquida - separação de moléculas entre uma fase estacionária (sólida) e uma fase móvel (liquida) dentro de uma coluna cromatográfica
Uso de diferentes cromatografias
Uso de troca iônica - eluição através de altas concentrações salinas
Depois coluna de interação hidrofóbica - meio já possui alta concentração salina
Interação - entre a proteína e resíduos hidrofóbicos presentes na matriz
Solução com alto teor de sal
ions nomeio removeram a camada de solvatação que a água forma ao redor da proteína - resíduos hidrofóbicos estão internos
Exposisão desses resíduos proporciona interação com a matriz
gradiente de concentração salina decrescente - elui primeiro proteínas com interação fraca, depois moderada e por ultimo elevada
Troca iônica - Resíduos de aminoácidos possuem cargas
Eluição utiliza solução com alta concentração de sal - pode afetar a estabilidade da proteína
Carga total da proteína depende do pH do meio (carga líquida) asociado ao ponto isoelétrico
pH menor que PI - carga líquida positiva
pH maior que PI - carga líquida negativa
Aplicação de campo elétrico para ocorrera migração diferencial das proteínas
Afinidade - Interação altamente específica entre a proteína e um ligante que estará presente na fase móvel
Técnica muito seletiva
Ex: resina absorvida com proteína A - se liga a porção não específica dos anticorpos (região Fc)
Retirada do Ac por meio:
3- adição de uma cauda polo A - afinidade com o níquel
2- fase móvel que interaja mais com a proteína A
1- alteração do pH da fase móvel - alterada levemente a forma da proteína
Exclusão molecular - separação por meio do peso molecular, forma e tamanho da molécula- maiores eluem primeiro e menores ficam mais tempo retidas na FE
Etapa 1- Rompimento da célula para liberação da proteína no meio
ELISA
Clonagem por diluição limite
Simples porém demorada - análise de centenas de clones
Principalmente glicosilação - adição de uma cadeia de carboidratos a um resíduo de aminoácido na proteína final
Padrão de glicosilação é espécie específica, podendo ter pequenas alterações mesmo em cels diferentes de uma mesma linhagem
Pode ser do tipo N-glicosilação ou O-glicosilação
São camadas de glicoformas - 2 ou mais moléculas de proteína produzidas pela mesma célula com micro diferenças no padrão
Controle de qualidade: faixas permitidas de cada glicoforma