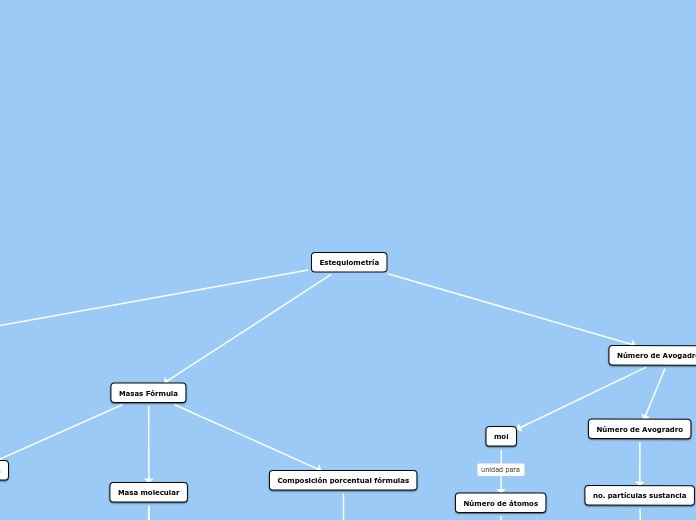
Estequiometría
Patrones Reactividad Química
Reacciones
Combinación
2 o más sustancias
un producto
A + B → C
metal + no metal
un sólido iónico
Descomposición
sustancia experimenta reacción
2 o más sustancias
Combustión
Reacciones rápidas
Producen una flama
O2 como reactivo
en nuestro cuerpo
Reacciones de oxidación
Masas Fórmula
Masa fórmula
suma de masas atómicas
átomos
fórmula química
Redondeamos MA a una cifra
uma
MF
Masa molecular
masa fórmula de
molécula
C6H1206
180.0 uma
MM
Composición porcentual fórmulas
Porcentaje en masa
contribuye cada elemento
sustancia
% = No. átomos x MA÷ MF * 100%
Número de Avogadro y Mol
mol
Número de átomos
cantidad de materia
tantos objetos
no. átomos en 12 g
Carbono 12
Número de Avogradro
no. partículas sustancia
en un mol
6.02 x 10ˆ23
NA
Amadeo Avogadro
Unidades recíprocas
6.02 x 10ˆ23 molˆ-1
y se lee
"mol inversa"
"por mol"
Masa molar
masa en gramos
mol de sustancia
NaCl
Masa fórmula (uma)
58.5 uma
Masa molar (g/mol)
58.5 g/mol
son numéricamente igual
Conversión
masas y moles
gramos a moles
Análisis
g sustancia y fórmula química
Calcular no. moles
moles a gramos
Análisis
No. moles y nombre sustancia
g de muestra
Masas y números partículas
Análisis
No. g y fórmula química
Ocupamos calcular
No. moléculas
No. átomos elemento