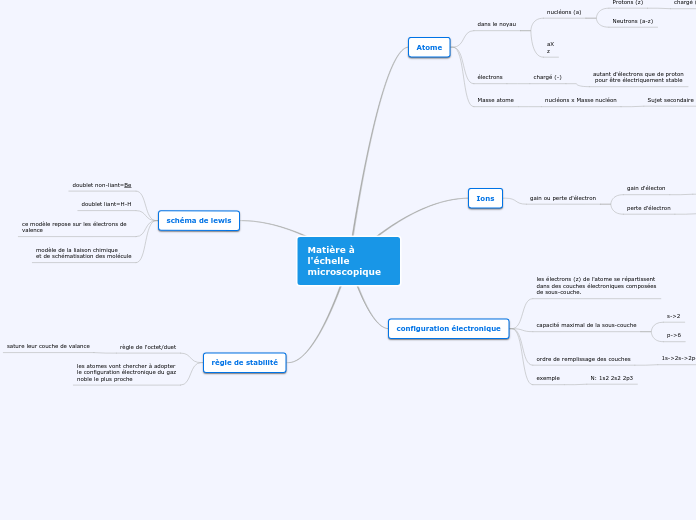
Matière à l'échelle microscopique
Atome
dans le noyau
nucléons (a)
Protons (z)
chargé (+)
Neutrons (a-z)
aX
z
électrons
chargé (-)
autant d'électrons que de proton
pour être électriquement stable
Masse atome
nucléons x Masse nucléon
Sujet secondaire
Ions
gain ou perte d'électron
gain d'électon
Ion négatif=anion
perte d'électron
Ion positif=cation
configuration électronique
les électrons (z) de l'atome se répartissent
dans des couches électroniques composées
de sous-couche.
capacité maximal de la sous-couche
s->2
p->6
ordre de remplissage des couches
1s->2s->2p->3s->3p...
exemple
N: 1s2 2s2 2p3
schéma de lewis
doublet non-liant=Be
doublet liant=H-H
ce modèle repose sur les électrons de valence
modèle de la liaison chimique
et de schématisation des molécule
règle de stabilité
règle de l'octet/duet
sature leur couche de valance
les atomes vont chercher à adopter
le configuration électronique du gaz
noble le plus proche