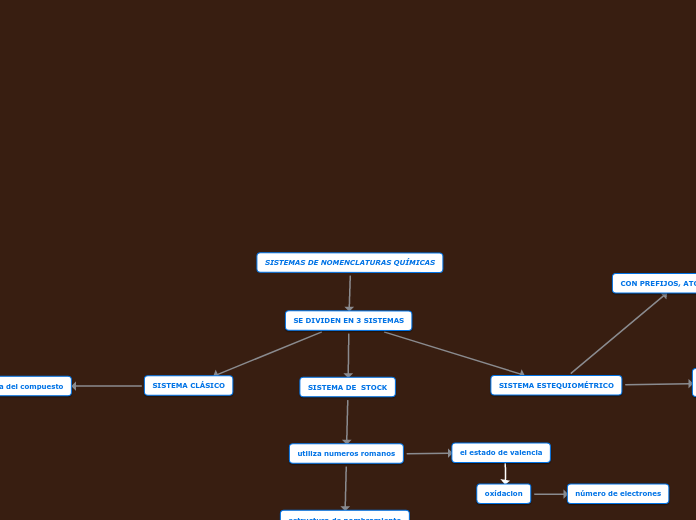
SISTEMAS DE NOMENCLATURAS QUÍMICAS
SE DIVIDEN EN 3 SISTEMAS
SISTEMA CLÁSICO
indica la valencia del compuesto
uso de prefijos y sufijos
reglas
1 de valencia
nombre+silaba "de"
ejemplo
K2O, óxido de potasio u óxido potásico
nombre+"ico"
2 de valencia
"oso" menor valencia
ejemplo
Fe2O3, Fe2+3O3-2, hierro con valencia 3, (estado de oxidación +3), óxido férrico
"ico" mayor valencia
ejemplo
FeO, Fe+2O-2, hierro con la valencia 2, (estado de oxidación +2), óxido ferroso
3 de valencia
"hipo-... -oso" menor valencia
ejemplo
P2O, P2+1O-2, fósforo con la valencia 1, (estado de oxidación +1), óxido hipofosforoso
"-oso" valencia intermedia
ejemplo
P2O3, P2+3O3-2, fósforo con valencia 3, (estado de oxidación +3), óxido fosforoso
"-ico" mayor valencia
ejemplo
P2O5, P2+5O5-2, fósforo con valencia 5, (estado de oxidación +5), óxido fosfórico
4 de valencia
"hipo- … -oso" valencia más pequeña
"-oso" valencia pequeña
"-ico" valencia grande
"per- … -ico" valencia más grande
5 de valencia
"hipo- … -oso" valencia más pequeña
"… -oso" valencia media-menor
"… -ico" la media
"per- … -ico" valencia media-mayor
"hiper- … -ico" valencia mayor
SISTEMA DE STOCK
utiliza numeros romanos
el estado de valencia
oxídacion
número de electrones
estructura de nombramiento
nombre genérico + "de" + nombre del elemento específico + el estado de oxidación.
ejemplo:
Fe2S3, Fe2+3S3-2, sulfuro de hierro (III)
SO3, S+6O3-2, óxido de azufre (VI)
SISTEMA ESTEQUIOMÉTRICO
CON PREFIJOS, ATOMICIDAD
USO DE PREFIJOS GRIEGOS PARA SU NOMBRAMIENTO
ETRUCTURA
prefijo-nombre genérico + prefijo-nombre específico
ejmplo:
CrBr3: tribromuro de cromo
CO: monóxido de carbono
tabla de clasificacion
PREFIJOS GRIECOS
numero de átomos
1
2
3
4
5
6
7
8
9
10
mono-
di-
tri-
tetra-
penta-
hexa-
hepta-
octa-
nona-
deca_