av Alejandra Blanco för 5 årar sedan
291
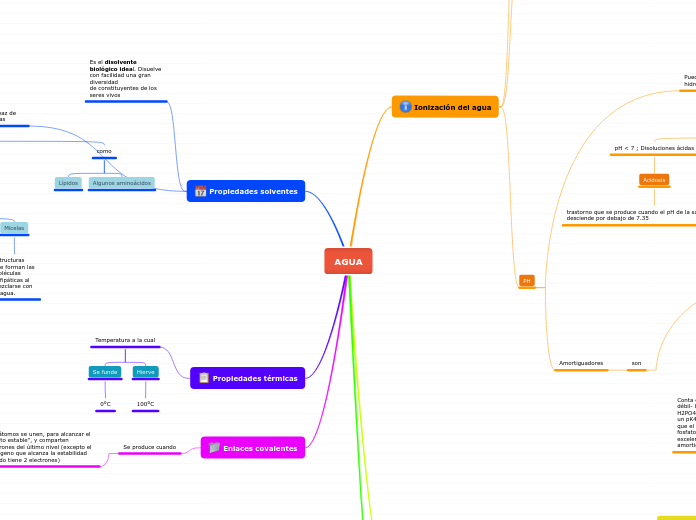
AGUA MAPA CYNTHIA BLANCO
av Alejandra Blanco för 5 årar sedan
291

Mer av detta
Type in the name of your subject.
Add detailed notes about each lecture, so that when the time comes to prepare for exams, you will have an easier and quicker overview.
Add a short description of the lecture.
Add here all the details about your projects.
100°C
0°C
Schedule your course ahead. Knowing all the information will make everything easier.
Algunos aminoácidos
Lípidos
Add class name.
Son virtualmente insolubles en agua
Add additional information about this class.
Micelas
Estructuras que forman las moléculas anfipáticas al mezclarse con el agua.
Esferas de solvatación
Los caparazones de las moléculas de agua se agrupan alrededor de los iones positivos y negativos. El tamaño de la esfera de solvatación depende de la densidad de carga del ion
Moléculas anfipaticas
Los ácidos grasos ionizados son moléculas anfipáticas debido a que contienen grupos carboxilato hidrófilos y grupos hidrocarburos hidrófobos
Add the class information for each week.
Review your resource requirements and tick off the devices you will need as well as their availability. Add others, if necessary.
Add other resources:
Fuerzas de van der Waals
son interacciones electrostáticas relativamente débiles que se originan cuando las biomoléculas que contienen dipolos permanentes neutros se aproximan entre sí o a un dipolo inducible (como una nube). Cuanto más polares y colineales son los grupos involucrados, más fuerte es la interacción de van der Waals.
existen 3 tipos
interacciones dipolo inducido dipolo inducido
Son las más débiles
interacciones dipolo-dipolo inducido
interacciones dipolo-dipolo
Son las más fuertes
Enlaces de hidrogeno
el hidrógeno es compartido de modo desigual por los dos centros electronegativos: núcleos de oxígeno en el caso de un par de moléculas de agua. El enlace tiene tanto carácter electrostático (iónico) como covalente.
Interacciones iónicas
electrostáticas ocurren entre cualesquiera de dos cargas opuestas parciales (moléculas polares) o bien, completas (iones o moléculas con carga).
Type in all the info you would like to know about this subject. If there is something you don't know yet, no problem! You can fill in the blanks along the way.
Did your teacher present the objectives of this course? Write them down and add anything else that might help you reach these objectives.
Sustancias que ayudan a mantener un ph óptimo para que una reacción se lleve a cabo, regulan los cambios bruscos en el ph.
Fisiológicos
proteínas
Formados por aminoácidos unidos por enlaces pépticos contienen varias cadenas laterales que pueden donar o aceptar protones.
bicarbonato
posee tres componentes
Después, el ácido carbónico se disocia muy rápido para formar iones H+ y HCO3−: H2CO3 7 H+ + HCO3− Bicarbonato
El primero de ellos, el dióxido de carbono, reacciona con el agua para formar ácido carbónico CO2 + H2O 7 H2CO3 Ácido carbónico
Fosfato
Conta de un par ácido débil- base conjugada H2PO4 −/HPO4 2− con un pK4 de 7.2 pareciera que el amortiguador de fosfato es una elección excelente para amortiguar la sangre
por lo tanto existen
pH > 7; Disoluciones básicas
Alcalosis
Cuando el pH aumenta por encima de 7.45.
pH = 7; Disoluciones neutras.
pH < 7 ; Disoluciones ácidas
Acidosis
trastorno que se produce cuando el pH de la sangre humana desciende por debajo de 7.35
Add details about your teachers' evaluation criteria. This way you will know the aspects you need to focus on.
Conjugada
es
El producto que ha perdido protones de la reacción de disociación.
Débil
Bases orgánicas que poseen una pequeña capacidad para combinarse con los iones hidrógeno
Write down the attendance policy, to avoid confusion throughout the year.
Un grupo lateral de una molécula es ácido si tiene la capacidad de donar protones
Ácido débil
son
Ácidos orgánicos que no se disuelven en su totalidad en el agua