av Santiago Burgos för 4 årar sedan
415
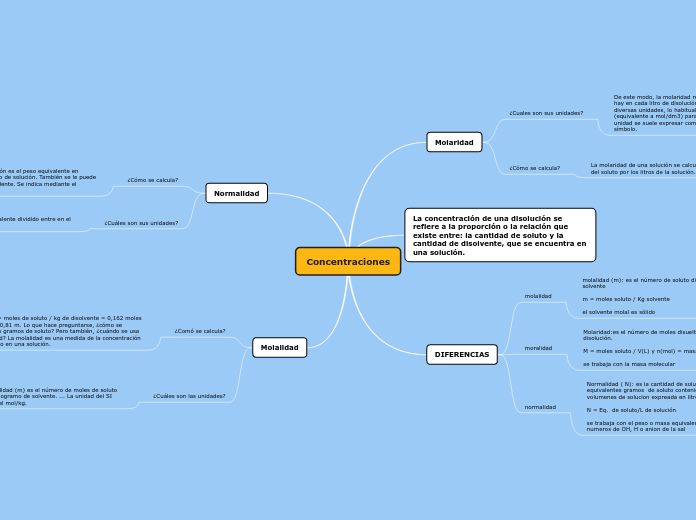
Concentraciones
av Santiago Burgos för 4 årar sedan
415

Mer av detta
¿Cuál es la molaridad de 58,5 gr de cloruro de sodio disueltos en 2 litros de solvente?.
Para poder hacer el cálculo tenemos que convertir gramos a moles. Si consideramos que el peso molecular del cloruro de sodio es: 58,5 [(peso del Cl- (35,5) + peso del Na+(23)] entonces esa cantidad es un mol. M= 1 M / 2L= 0,5 M.
Ejemplo 1: calcular la molalidad de una disolución de ácido sulfúrico H2SO4 siendo la masa del disolvente de 600 gramos y la cantidad de ácido de 60 gramos. Datos: peso molecular del H2SO4 = 98 gramos / mol. En primer lugar calculamos el número de moles y a partir de ahí obtenemos la molalidad: n de H2SO4 = masa / peso molecular =60 gramos / 98 gramos · mol-1 = 0,61 moles m = n / masa disolvente = 0,61 moles / 0,6 kg = 1,02 molal
Ejemplo
un ácido sulfúrico 1 M (H 2 SO 4 ) es 2 N para reacciones ácido-base porque cada mol de ácido sulfúrico proporciona 2 moles de iones H + . El ácido sulfúrico 1 M es 1 N para la precipitación de sulfato, ya que 1 mol de ácido sulfúrico proporciona 1 mol de iones sulfato.