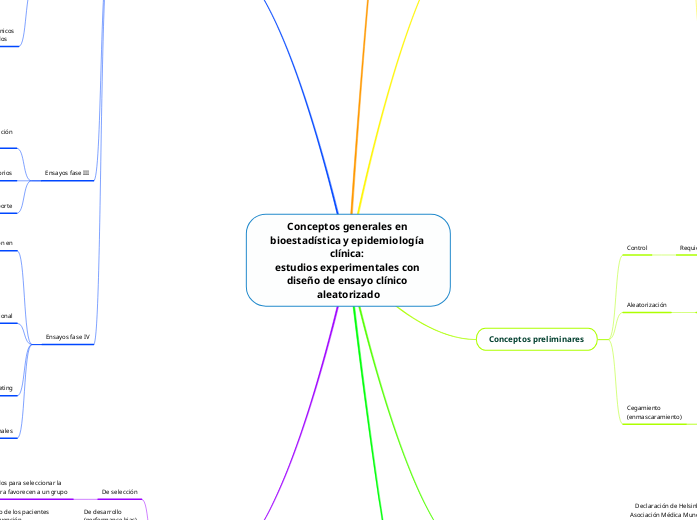
Conceptos generales en bioestadística y epidemiología clínica:
estudios experimentales con diseño de ensayo clínico
aleatorizado
Tipos de estudios
experimentales
en seres humanos
Ensaro clínico aleatorizado clásico
Aleatoriza pacientes
que reciben una intervención
Estudios cuasi-experimentales
No presenta un proceso de aleatorización
Estudios experimentales con
controles externos o históricos
Grupo control de diferente población
Medidas de asociación
Diseño prospectivo
Riesgo Relativo
RR
Razón de los riesgos entre
Expuestos
No expuestos
Igual a 1
No existe asociación
Mayor a 1
La intervención aumenta
la probabilidad del
desenlace
Menor a 1
La intervención disminuye
la probabilidad del desenlace
Reducción absoluta
de riesgo (RAR)
Diferencia de riesgos
Grupo control
Grupo intervención
Reducción de riesgo
Atribuida a intervención
Resultado negativo
Aumento absoluto de riesgo
Número necesario a tratar
Reducción relativa
de riesgo
Diferencia de riesgos
RAR
Entre control (no expuestos)
Resultado negativo
Aumento relativo del riesgo
Frecuente sobreestimación
Efectos del tratamiento
Reportar RAR cuando
sea posible
Conceptos preliminares
Control
Requiere
Comparación
estadísticamente
válida
Entre
Grupo intervención
Grupo control
Dos grupos
Pacientes
Voluntarios sanos
Aleatorización
Método de control
Sesgos
Investigación
Cegamiento
(enmascaramiento)
Pueden ser
Abiertos
No ciegos
Conocen intervención
Investigador
Participante
Ciegos
Desconocen intervención
Ciego simple
Participante desconoce
Doble ciego
Participante/investigador
Triple ciego
Participante/investigador/evaluador
Intervención
Fármaco
Placebo
Activos
Imitan a la
intervención
Principio activo
Aspectos bioéticos y
registro del protocolo
Declaración de Helsinki
Asociación Médica Mundial
1964
Repositorios disponibles
Clinical Trials
USA
ISRCTN
Europa
Cochrane Central Register
of Controlled Trials
Cochrane
ICTRP
OMS
Componentes y procedimientos
esenciales en los ensayos clínicos
Reclutamiento y aleatorización
de pacientes
Contol de sesgos
De selección
De confusión
Medición de resultados
Metodos de enmascaramiento
Ciego de pacientes
Efecto placebo
Efecto nocebo
Efecto Hawthorne
Previene el sesgo de medición
Análisis de datos
Incluye a todos/mayoría
de participantes aleatorizados
Análisis primario
Analiza pacientes como
parte del grupo original
Análisis por intención
de tratar
Baja adherencia
Se excluye pacientes
Clasificación de
Ensayos Clínicos
Estudios preclínicos
Detección
Problemas de seguridad
del producto
Carcinogenicidad
Teratogenicidad
Involucran
Procesos
Síntesis química
Pruebas biológicas
Estudios toxicológicos
Ensayos fase I
Estudios farmacológicos
(sin objetivo terapéuticos)
Evalúan
Toxicidad
Parametros
farmacocinéticos
Parametros
farmacodinámicos
Tolerancia
Respuesta a distintas dosis
dosis máxima segura
Se realizan en
Voluntarios sanos
Pacientes con enfermedad
Sin otra posibilidad
de tratamiento
Abiertos no controlados
>100 pacientes
Primeras pruebas en humanos
Ensayos fase II
Primera exploración clínica
del tratamiento
Define
Posología
Aportan
Información preliminar
Eficacia
Seguriada clínica
Se realizan
Pacientes portadores
Enfermedad
Con grupo control
Opcional
Ensayos clínicos
aleatorizados
100-300 participantes
Fase II temprana
IIa
Estudio piloto
Evalúa
Perfil de seguridad
Biodisponibilidad
Fase II tardía
IIb
Garantiza
Seguridad del
fármaco
Evalúa
Superioridad vs
otros fármacos
Ensayos fase III
Estudio de confirmación
terapéutica
Multicentrico
Muestra
>300 participantes
Estudios pivotales/confirmatorios
Estimación del tamaño muestral
Asociado
Hipótesis
Soporte
Autorización del registro
Comercialización del fármaco
Ensayos fase IV
Evaluación en
Distintas poblaciones
Información adicional
Riesgos
Efectos adversos
Beneficios
Nuevos usos
Farmacovigilancia
Interacciones farmacológicas
Postmarketing
Estudios observacionales
Series de casos
Casos y controles
Estudios de cohorte
Sesgos
De selección
métodos para seleccionar la
muestra favorecen a un grupo
De desarrollo
(performance bias)
Seguimiento estricto de los pacientes
asignados a la intervención
De detección o
información
desenlace en estudio es
“detectado” entre los grupos
De desgaste o
post aleatorización
(attrition bias)
diferencias sistemáticas
en el seguimiento
De reporte
(reporting bias)
Se evalua mediante la revisión del
registro inicial del ensayo clínico