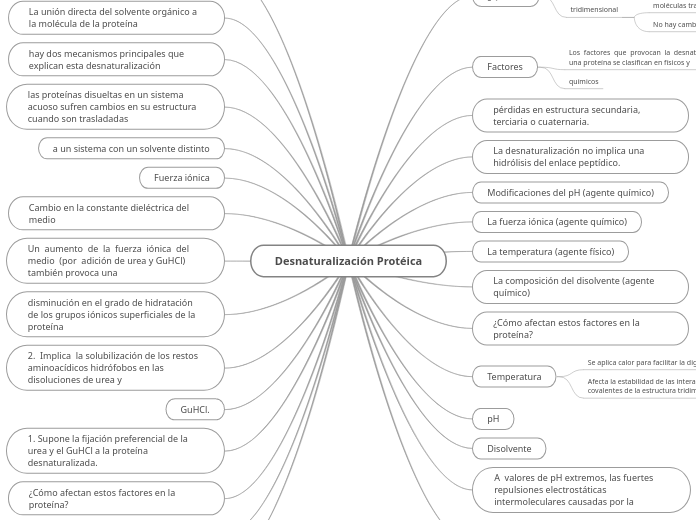
Desnaturalización Protéica
La estructuración se aleja de la forma nativa debido a un cambio en su conformación
conllevando un aumento en la entropía de las moléculas trayendo como consecuencia
No hay cambios en la estructura primaria
Los factores que provocan la desnaturalización de una proteína se clasifican en físicos y
pérdidas en estructura secundaria, terciaria o cuaternaria.
La desnaturalización no implica una hidrólisis del enlace peptídico.
Modificaciones del pH (agente químico)
La fuerza iónica (agente químico)
La temperatura (agente físico)
La composición del disolvente (agente químico)
¿Cómo afectan estos factores en la proteína?
Se aplica calor para facilitar la digestión de proteínas
Afecta la estabilidad de las interacciones no-covalentes de la estructura tridimensional
A valores de pH extremos, las fuertes repulsiones electrostáticas intermoleculares causadas por la
elevada carga neta determinan el hinchamiento y el desplegamiento de las moléculas proteicas
A pH neutro, la mayor parte de las proteínas están negativamente cargadas.
La unión directa del solvente orgánico a la molécula de la proteína
hay dos mecanismos principales que explican esta desnaturalización
las proteínas disueltas en un sistema acuoso sufren cambios en su estructura cuando son trasladadas
a un sistema con un solvente distinto
Cambio en la constante dieléctrica del medio
Un aumento de la fuerza iónica del medio (por adición de urea y GuHCl) también provoca una
disminución en el grado de hidratación de los grupos iónicos superficiales de la proteína
2. Implica la solubilización de los restos aminoacídicos hidrófobos en las disoluciones de urea y
1. Supone la fijación preferencial de la urea y el GuHCl a la proteína desnaturalizada.
¿Cómo afectan estos factores en la proteína?
Por adición de clorhidrato de guanidina