作者:SantanaGamer 323 4 年以前
377
Organigrama arbol
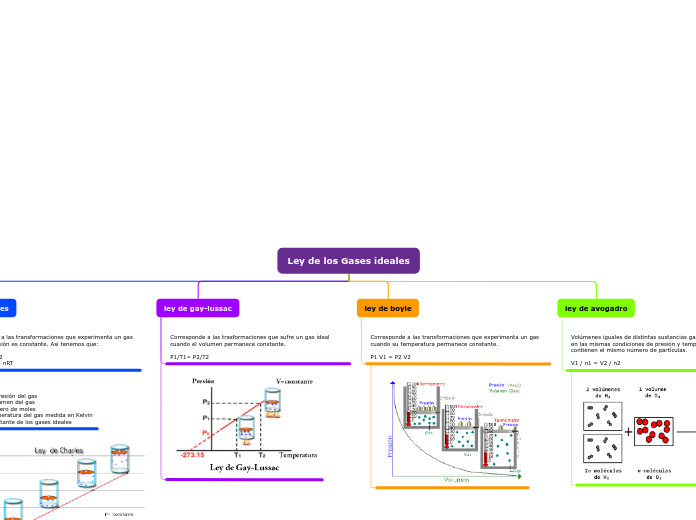
Las leyes de los gases ideales explican el comportamiento de los gases bajo diferentes condiciones. La ley de Boyle describe cómo un gas se transforma a temperatura constante, indicando que la presión y el volumen son inversamente proporcionales.