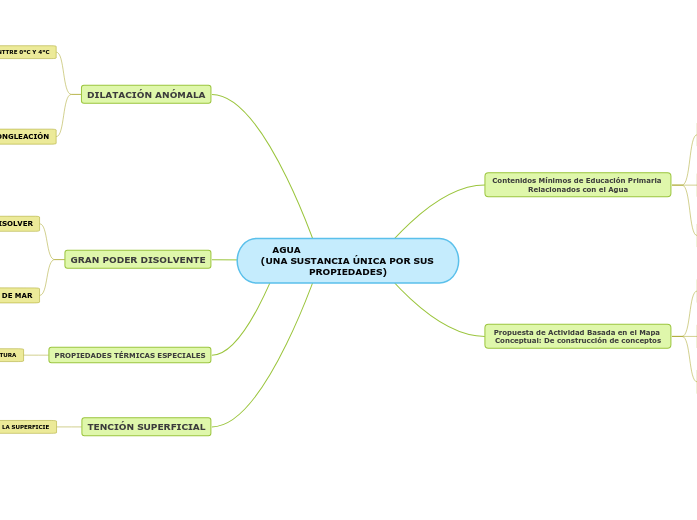
AGUA (UNA SUSTANCIA ÚNICA POR SUS PROPIEDADES)
Contenidos Mínimos de Educación Primaria Relacionados con el Agua
Características Básicas del Agua
Propiedades Generales del Agua
Propiedades Físicas y Químicas del Agua
Impacto en la Naturaleza y el Clima
Ciclo del Agua y Conservación del Agua
Importancia de la Conservación del Agua
Propuesta de Actividad Basada en el Mapa Conceptual: De construcción de conceptos
Ciclo del Agua y Conservación del Agua
- Comprender el agua como "disolvente universal".
- Observar cómo la temperatura afecta la disolución
Los estudiantes experimentarán con el agua como disolvente. Usarán sal y azúcar para ver cómo se disuelven en agua fría y caliente, observando la diferencia.
DILATACIÓN ANÓMALA
CALENTAMIENTO ENTTRE 0ºC Y 4ºC
PROCESO: Cuando el agua se calienta en este rango, su densidad aumenta hasta alcanzar un máximo a los 4°C.
Consecuencia: A partir de 4°C, el agua sigue el comportamiento esperado de otros líquidos, disminuyendo su densidad al aumentar su temperatura.
Importancia: La densidad máxima del agua a 4°C permite que en climas fríos, el agua más cálida permanezca en el fondo de lagos y ríos, ayudando a la supervivencia de especies acuáticas.
ENFRIAMIENTO Y CONGLEACIÓN
Proceso: Al enfriarse por debajo de 4°C y congelarse, el agua forma estructuras hexagonales huecas, lo cual disminuye su densidad.
Consecuencia: Esta estructura hexagonal hace que el hielo flote sobre el agua líquida, lo que aísla térmicamente el agua bajo la capa de hielo y protege la vida acuática en invierno.
GRAN PODER DISOLVENTE
CAPACIDAD DE DISOLVER
El agua es capaz de disolver más sustancias que cualquier otro líquido, excepto sustancias oleaginosas (grasas, aceites, ceras).
Ejemplo: Disuelve minerales, gases (como oxígeno y dióxido de carbono), alcoholes, y diversas sales.
Importancia Biológica: Esta capacidad permite a los seres acuáticos vivir en ambientes con nutrientes disueltos necesarios para procesos vitales como la respiración y la fotosíntesis.
COMPOSICOÓN DEL AGUA DE MAR
Ejemplo: En cada kilogramo de agua de mar, hay aproximadamente 965 g de agua pura y 35 g de sales disueltas, como cloro, sodio, sulfatos, magnesio, calcio, y otros elementos en menor cantidad (bicarbonatos, bromo, boro, etc.).
PROPIEDADES TÉRMICAS ESPECIALES
RESISTENCIA A CAMBIOS DE TEMPERATURA
Característica: El agua tiene un calor específico alto, lo cual significa que necesita absorber o liberar gran cantidad de calor para variar su temperatura.
Consecuencia: Este alto calor específico estabiliza la temperatura del agua y regula el clima, especialmente en zonas costeras.
TENCIÓN SUPERFICIAL
ATRACCIÓN MOLECULAR EN LA SUPERFICIE
Proceso: Las moléculas de agua en la superficie se atraen entre sí, formando una lámina tensa como si fuera una membrana elástica.
Consecuencia: Esta lámina tensa permite que ciertos insectos, como el zapatero, puedan caminar sobre el agua sin hundirse.
Ejemplo de Tensión Superficial en Acción
Insectos: La tensión superficial permite a los insectos sostenerse en la superficie del agua.
Efecto "Planchazo": Cuando una persona cae de espaldas al agua, la tensión superficial genera una resistencia que produce una sensación de impacto.