af Mateus Carvalho 4 år siden
254
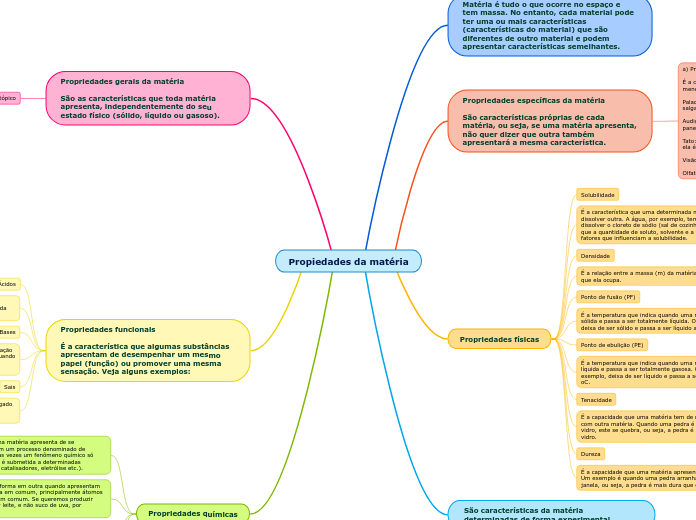
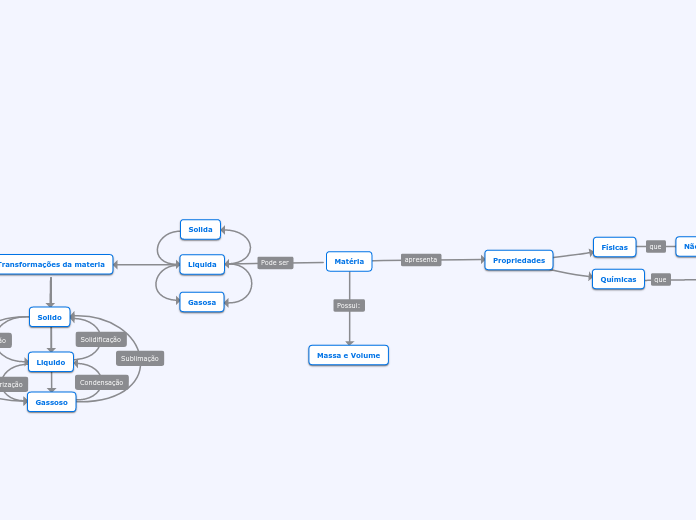
Propiedades da matéria
As propriedades da matéria podem ser divididas em funcionais e específicas. As propriedades funcionais referem-se às características que certas substâncias exibem ao desempenhar funções semelhantes ou promover sensações específicas, como os sabores salgado, adstringente e azedo de bases, substâncias básicas e ácidas, respectivamente, todas com a capacidade de dissociação ou ionização em água.