Текущая тема
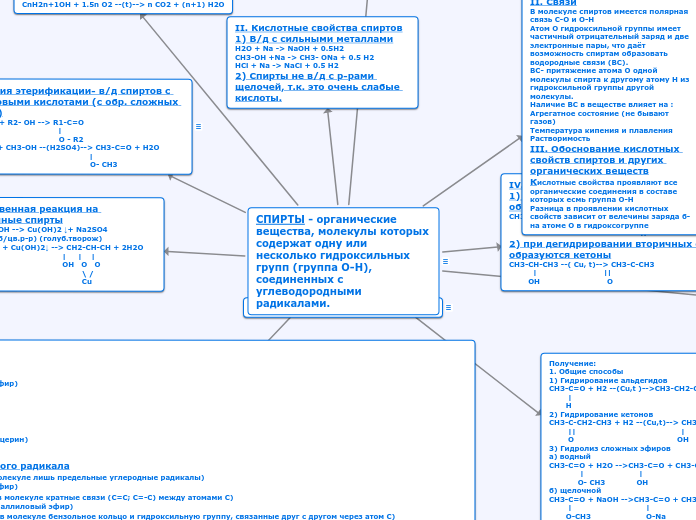
СПИРТЫ - органические вещества, молекулы которых содержат одну или несколько гидроксильных групп (группа O-H), соединенных с углеводородными радикалами.
Физическе свойства
I. Агрегатное состояние
Все спирты ядовиты. Низшие спирты имеют характерный "спиртовой запах".
C1-C10- средние и низшие спирты (жидкости) имеют алкогольный запах и жгучий вкус, хорошо растворим в воде.
C11-...-высшие спирты (твердые вещества).
II. Связи
В молекуле спиртов имеется полярная связь C-O и O-H
Атом O гидроксильной группы имеет частичный отрицательный заряд и две электронные пары, что даёт возможность спиртам образовать водородные связи (ВС).
ВС- притяжение атома O одной молекулы спирта к другому атому H из гидроксильной группы другой молекулы.
Наличие ВС в веществе влияет на :
Агрегатное состояние (не бывают газов)
Температура кипения и плавления
Растворимость
III. Обоснование кислотных свойств спиртов и других органических веществ
Кислотные свойства проявляют все органические соединения в составе которых есмь группа O-H
Реакция в проявлении кислотных свойств зависит от велечины заряда б- на атоме O в гидроксогруппе
Получение:
1. Общие способы
1) Гидрирование альдегидов
CH3-C=O + H2 --(Cu,t )-->CH3-CH2-OH
|
H
2) Гидрирование кетонов
CH3-C-CH2-CH3 + H2 --(Cu,t)--> CH3-CH-CH2-CH3
|| |
O OH
3) Гидролиз сложных эфиров
а) водный
CH3-C=O + H2O -->CH3-C=O + CH3-OH
| |
O- CH3 OH
б) щелочной
CH3-C=O + NaOH -->CH3-C=O + CH3-OH
| |
O-CH3 O-Na
2. Получение гликолей
1) Мягкое окисление алкенов
CH2=CH2 + KMnO4+ H2O --> 0 CH2-CH2 + MnO2+KOH
| |
OH OH
2) В/д алкенов с перекисью водорода
CH2=CH2 + H2O2 --> CH2-CH2
| |
OH OH
3. Специфические способы
1) Метанол получают из синтез-газа
CO + 2H2 --(t,p, Fe3O4)--> CH3-OH
2) Этанол- спиртовое брожение глюкозы
C6H12O6--(дрожжи)--> 2C2H5OH + 2CO2
4. Восстановление сложных эфиров
CH3-CH2-C=O +2H2 --( t,кат)--> CH3-CH2-CH2-OH + CH3-OH
|
O- CH3
Изомерия
I. Положение -O-H группы
CH3-CH2-CH2-OH CH3-CH2-CH3 пропанол-2
пропанол-1 |
OH
II. Углеродного скелета
CH3-CH2-CH2-CH2-OH CH3-CH-CH2-OH 2-метилпропанол-1
бутанол-1 |
CH3
III. Межклассовая изомерия (с простыми эфирами)
CH3-CH2-OH CH3-O-CH3
этанол диметиловый эфир
IV.Цис-транс изомерия
CH3-CH=CH-OH пропен-2ол-1
CH3 OH H OH
\ / \ /
C=C C=C
/ \ / \
H H CH3 H
цис-пропен-2-ол-1 транс-пропен-2-ол-1
Изомерия
I. Положение -O-H группы
CH3-CH2-CH2-OH CH3-CH2-CH3 пропанол-2
пропанол-1 |
OH
II. Углеродного скелета
CH3-CH2-CH2-CH2-OH CH3-CH-CH2-OH 2-метилпропанол-1
бутанол-1 |
CH3
III. Межклассовая изомерия (с простыми эфирами)
CH3-CH2-OH CH3-O-CH3
этанол диметиловый эфир
IV.Цис-транс изомерия
CH3-CH=CH-OH пропен-2ол-1
CH3 OH H OH
\ / \ /
C=C C=C
/ \ / \
H H CH3 H
цис-пропен-2-ол-1 транс-пропен-2-ол-1
Физическе свойства
I. Агрегатное состояние
Все спирты ядовиты. Низшие спирты имеют характерный "спиртовой запах".
C1-C10- средние и низшие спирты (жидкости) имеют алкогольный запах и жгучий вкус, хорошо растворим в воде.
C11-...-высшие спирты (твердые вещества).
II. Связи
В молекуле спиртов имеется полярная связь C-O и O-H
Атом O гидроксильной группы имеет частичный отрицательный заряд и две электронные пары, что даёт возможность спиртам образовать водородные связи (ВС).
ВС- притяжение атома O одной молекулы спирта к другому атому H из гидроксильной группы другой молекулы.
Наличие ВС в веществе влияет на :
Агрегатное состояние (не бывают газов)
Температура кипения и плавления
Растворимость
III. Обоснование кислотных свойств спиртов и других органических веществ
Кислотные свойства проявляют все органические соединения в составе которых есмь группа O-H
Разница в проявлении кислотных свойств зависит от велечины заряда б- на атоме O в гидроксогруппе
VI. Качественная реакция на многоатомные спирты
CuSO4 + 2NaOH --> Cu(OH)2 ↓+ Na2SO4
(голуб.р-р) (б/цв.р-р) (голуб.творож)
CH2-CH2-CH2 + Cu(OH)2↓ --> CH2-CH-CH + 2H2O
| | | | | |
OH OH OH OH O O
\ /
Cu
III. Дегидратация
1) Межмолекулярная(с обр. простых эфиров)
CH3-OH + CH3-CH2-OH--( H2SO4, t<140)--> CH3-O-CH2-CH3
2) Внутримолекулярная (с обр. алкена)
CH3-CH-CH2-CH3--(H2SO4, t>140)-->CH3-CH=CH-CH3
|
OH
Классификация
I. По атомности
1.Одноатомные
CH3-CH2-OH (этанол; этиловый эфир)
2.Двуатомные (гликоли)
CH2-CH2 (этанол-1,2)
| |
OH OH
3.Трехатомные
CH2-CH-CH2 (пропанол-1,2,3; глицерин)
| | |
OH OH OH
II. По характеру углеродного радикала
1.Предельные (содержат в молекуле лишь предельные углеродные радикалы)
CH3-CH2-OH (этанол; этиловый эфир)
2.Непредельные (содержат в молекуле кратные связи (С=C; C=-C) между атомами C)
CH2=CH-CH2-OH (пропен-2-ол-1; аллиловый эфир)
3.Ароматические (содержат в молекуле бензольное кольцо и гидроксильную группу, связанные друг с другом через атом C)
OH ФЕНОЛ НЕ ЯВЛЯЕТСЯ СПИРТОМ
|
/ \
| 0 |
\ /
БЕНЗИЛОВЫЙ СПИРТ - ПРОСТЕЙШИЙ АРОМАТИЧЕСКИЙ СПИРТ
CH2-OH
/ \ /
| 0 |
\ /
II. По характеру атома С
1.Первичные 2.Вторичные 3.Третичные
(в молекулах которых гидроксильная (в молекулах которых гидроксильная (в молекулах которых гидроксильная группа связана с первичным атомом С) группа связана с вторичным атомом С) группа связана с третичным атомом С)
CH2-R R-CH-R1 R3
| | |
OH OH R-C-R1
|
OH
III. По характеру атома С
1.Первичные 2.Вторичные 3.Третичные
(в молекулах которых гидроксильная (в молекулах которых гидроксильная (в молекулах которых гидроксильная
группа связана с первичным атомом С) группа связана с вторичным атомом С) группа связана с третичным атомом С)
CH2-R R-CH-R1 R3
| | |
OH OH R-C-R1
|
OH
V.Реакция этерификации- в/д спиртов с карбоновыми кислотами (с обр. сложных эфиров)
R1- C = O + R2- OH --> R1-C=O
| |
OH O - R2
CH3-C=O + CH3-OH --(H2SO4)--> CH3-C=O + H2O
| |
OH O- CH3
VI. Качественная реакция на многоатомные спирты
CuSO4 + 2NaOH = Cu(OH)2 ↓+ Na2SO4
(голуб.р-р) (б/цв.р-р) (голуб.творож)
CH2-CH2-CH2 + Cu(OH)2↓ = CH2-CH-CH + 2H2O
| | | | | |
OH OH OH OH O O
\ /
Cu
IV. Окисление- дегидрирование
1) при дегидрировании первичных спиртов образуются альдегиды
CH3-CH2-CH2-OH --(Сu,t)--> CH3-CH2-C=O + H2
|
H
2) при дегидрировании вторичных спиртов образуются кетоны
СH3-CH-CH3 --( Cu, t)--> CH3-C-CH3
| ||
OH O
II. Кислотные свойства спиртов
1) В/д с сильными металлами
H2O + Na -> NaOH + 0.5H2
CH3-OH +Na -> CH3- ONa + 0.5 H2
HCl + Na -> NaCl + 0.5 H2
2) Спирты не в/д с р-рами щелочей, т.к. это очень слабые кислоты.
Химические свойства:
I. Горение
CnH2n+1OH + 1.5n O2 --(t)--> n CO2 + (n+1) H2O
Получение:
1. Общие способы
1) Гидрирование альдегидов
CH3-C=O + H2 =Cu,t CH3-CH2-OH
|
H
2) Гидрирование кетонов
CH3-C-CH2-CH3 + H2 =Cu,t CH3-CH-CH2-CH3
|| |
O OH
3) Гидролиз сложных эфиров
а) водный
CH3-C=O + H2O = CH3-C=O + CH3-OH
| |
O- CH3 OH
б) щелочной
CH3-C=O + NaOH = CH3-C=O + CH3-OH
| |
O-CH3 O-Na
2. Получение гликолей
1) Мягкое окисление алкенов
CH2=CH2 + KMnO4+ H2O = 0 CH2-CH2 + MnO2+KOH
| |
OH OH
2) В/д алкенов с перекисью водорода
CH2=CH2 + H2O2 = CH2-CH2
| |
OH OH
3. Специфические способы
1) Метанол получают из синтез-газа
CO + H2 =t,p, Fe3O4 CH3-OH
2) Этанол- спиртовое брожение глюкозы
C6H12O6=дрожжи 2C2H5OH + 2CO2
4. Восстановление сложных эфиров
CH3-CH2-C=O +2H2 = t,кат CH3-CH2-CH2-OH + CH3-OH
|
O- CH3
Общая формула: CnH2n+2O или CnH2n+1OH
Классификация
I. По атомности
Одноатомные
CH3-CH2-OH (этанол; этиловый эфир)
CH3-OH (метанол; метиловый эфир)
Двуатомные (гликоли)
CH2-CH2-CH2 (пропандиол-1,3)
| |
OH OH
CH2-CH2 (этандиол-1,2)
| |
OH OH
Трехатомне
CH2-CH-CH2 (пропантриол-1,2,3; глицерин)
| | |
OH OH OH
II. По характеру углеродного радикала
Предельные
CH3-CH2-OH (этанол; этиловый эфир)
Непредельные
CH2=CH-CH2-OH (пропен-2-ол-1; аллиловый эфир )
Ароматические