von ANNE SALOME LUNA JIMENEZ Vor 2 Jahren
391
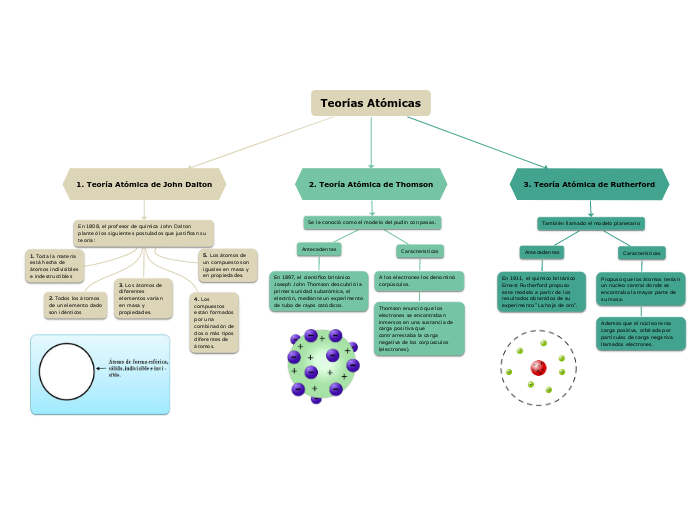
Tarea N°1: Teoría atómica de Dalton, Thomson y Rutherford
A lo largo de la historia, varios científicos han desarrollado teorías para entender la estructura del átomo. En 1808, John Dalton propuso que toda la materia está compuesta de átomos indivisibles e indestructibles, y que los átomos de cada elemento son idénticos en masa y propiedades.