por Ignacio Santana hace 4 años
388
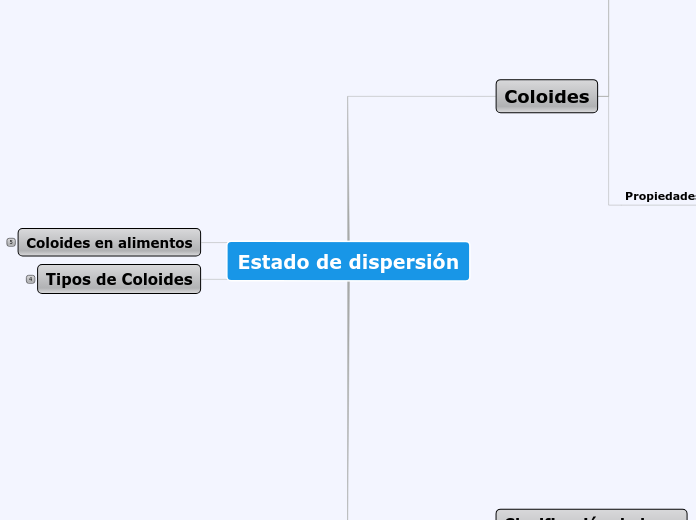
Estado de dispersión
Los coloides son sistemas de fases múltiples no homogéneos que se componen de una o más fases dispersas o discontinuas, llamadas micelas, en una fase continua. Estas partículas varían en tamaño de 1nm a 1um y no se difunden a través de membranas semipermeables ni presentan presión osmótica.