Topic flotante
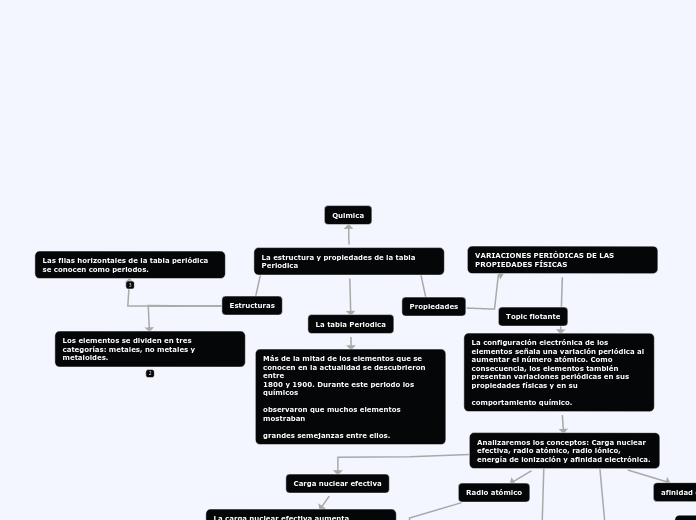
La estructura y propiedades de la tabla Periodica
Quimica
La tabla Periodica
Más de la mitad de los elementos que se
conocen en la actualidad se descubrieron entre
1800 y 1900. Durante este periodo los químicos
observaron que muchos elementos mostraban
grandes semejanzas entre ellos.
Propiedades
VARIACIONES PERIÓDICAS DE LAS PROPIEDADES FÍSICAS
La configuración electrónica de los elementos señala una variación periódica al
aumentar el número atómico. Como consecuencia, los elementos también
presentan variaciones periódicas en sus propiedades físicas y en su
comportamiento químico.
Analizaremos los conceptos: Carga nuclear efectiva, radio atómico, radio iónico,
energía de ionización y afinidad electrónica.
Radio atómico
Muchas propiedades físicas, incluidas la densidad y los puntos de fusión y ebullición, se relacionan con el tamaño de los
átomos. El tamaño de un átomo en términos de su radio atómico, que es la mitad de la longitud entre los núcleos de dos
átomos metálicos adyacentes o de una molécula diatómica.
energía de ionización
Las propiedades químicas de cualquier átomo se
determinan a partir de la configuración de los electrones
de valencia de sus átomos.
afinidad electrónica.
Otra propiedad de los átomos que influye en su comportamiento
químico es su capacidad para aceptar uno o más electrones
radio iónico
El radio iónico es el radio de un catión o un anión. El radio iónico
afecta las propiedades físicas y químicas de un compuesto iónico. Por
ejemplo, la estructura tridimensional de un compuesto iónico depende
del tamaño relativo de sus cationes y aniones.
Carga nuclear efectiva
La carga nuclear efectiva aumenta conforme descendemos
por un grupo periódico en particular y cuando nos movemos a
través de cualquier periodo de la tabla.
Estructuras
Los elementos se dividen en tres categorías: metales, no metales y metaloides.
Un no metal generalmente es mal conductor del calor y la electricidad.
Un metaloide presenta propiedades intermedias entre los metales y los no metales.
Un metal es un buen conductor del calor y la electricidad. Todos los elementos metálicos
comparten propiedades características, como el brillo y la alta conductividad eléctrica y calorífica;
y todos ellos, excepto el mercurio (Hg), son sólidos a temperatura ambiente
Las filas horizontales de la tabla periódica se conocen como periodos.
Las columnas (verticales) son grupos. La Unión Internacional de Química Pura y Aplicada (International
Union of Pure and Applied Chemistry, IUPAC) propuso la convención de numerar los grupos del 1 al 18 sin
designaciones A o B
El sexto periodo es de 32 elementos, pero para que estos ocupen una sola página, 14 de esos elementos
(aquellos con números atómicos del 57 al 70) se presentan en la parte inferior de la tabla.
El primer periodo solo tiene dos
elementos: hidrógeno (H) y helio (He). El segundo y tercer periodos consisten en ocho elementos cada uno.