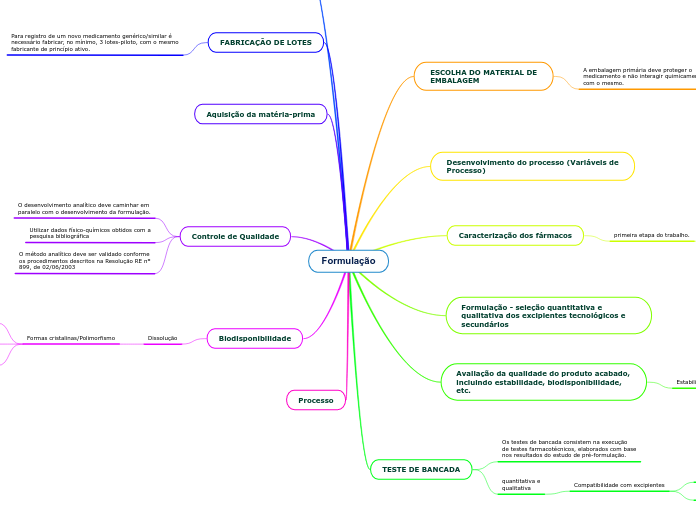
Formulação
ESCOLHA DO MATERIAL DE
EMBALAGEM
A embalagem primária deve proteger o
medicamento e não interagir quimicamente
com o mesmo.
Desenvolvimento do processo (Variáveis de
Processo)
Caracterização dos fármacos
primeira etapa do trabalho.
Solubilidade, perfil de solubilidade do fármaco, Constante de dissociação (pka), influência do pH e da temperatura, velocidade de dissolução
Os fármacos lipossolúveis;são normalmente
absorvidos após administração oral.
Moléculas polares;são pouco absorvidas após
administração oral.
Formulação - seleção quantitativa e qualitativa dos excipientes tecnológicos e secundários
Avaliação da qualidade do produto acabado,
incluindo estabilidade, biodisponibilidade, etc.
Estabilidade
Visa estabelecer as principais alterações ou
fatores de instabilidade do fármaco; como luz, temperatura, ph e entre outros
TESTE DE BANCADA
Os testes de bancada consistem na execução
de testes farmacotécnicos, elaborados com base
nos resultados do estudo de pré-formulação.
quantitativa e
qualitativa
Compatibilidade com excipientes
Tecnológicos ou primários
Específicos ou Secundários
ESTABILIDADE
Os resultados destes estudos irão definir o
prazo de validade e as condições de
armazenamento do produto
FABRICAÇÃO DE LOTES
Para registro de um novo medicamento genérico/similar é
necessário fabricar, no mínimo, 3 lotes-piloto, com o mesmo
fabricante de princípio ativo.
Aquisição da matéria-prima
Controle de Qualidade
O desenvolvimento analítico deve caminhar em
paralelo com o desenvolvimento da formulação.
Utilizar dados físico-químicos obtidos com a
pesquisa bibliográfica
O método analítico deve ser validado conforme
os procedimentos descritos na Resolução RE nº
899, de 02/06/2003
Biodisponibilidade
Dissolução
Formas cristalinas/Polimorfismo
Tamanho e formato das partículas
Formas cristalinas/Polimorfismo
Impacto na formulação, estabilidade, solubilidade e
Biodisponibilidade
Higroscopicidade