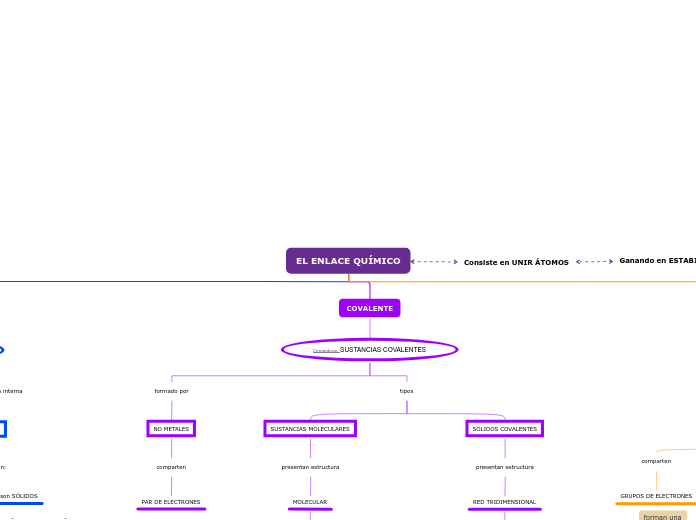
EL ENLACE QUÍMICO
IÓNICO
Creandose SUSTANCIAS IÓNICAS
formado por
METALES
pierden e-
CATIONES
NO METALES
ganan e-
ANIONES
presentas estructura interna
RED IÓNICA
formada por
ANIONES
CATIONES
Las propiedades son:
* A tª ambiente son SÓLIDOS
Puntos de FUSIÓN y EBULLICIÓN muy ALTOS
* Provocan que sean DURAS
* Conducción de electricidad
SI
ESTADO FLUIDO
NO
ESTADO SÓLIDO
EJEMPLOS
Sal común ( NaCl)
MgF2
KI
COVALENTE
Creandose SUSTANCIAS COVALENTES
formado por
NO METALES
comparten
PAR DE ELECTRONES
tipos
SUSTANCIAS MOLECULARES
presentan estructura
MOLECULAR
Las propiedades son:
* A tª ambienteson LIQUIDOS
Puntos de FUSIÓN y EBULLICIÓN muy BAJOS
*Poco solubles en AGUA
*NO conducen el calor ni electricidad
EJEMPLOS:
H2O
SOLIDOS COVALENTES
presentan estructura
RED TRIDIMENSIONAL
Las propiedades son:
*A tª ambiente son SÓLIDOS
Puntos de FUSIÓN y EBULLICIÓN muy ALTOS
Son muy DUROS
*Insolubles en agua
*NO conducen calor ni electricidad
EJEMPLOS:
SiO2
Diamante
METÁLICO
Creandose SUSTANCIAS METÁLICAS
formado por
METALES
comparten
GRUPOS DE ELECTRONES
su estructura es
RED METÁLICA
NUBE ELECTRÓNICA
Las propiedades
* A tª ambiente suelen ser SÓLIDOS
Puntos de FUSIÓN y EBULLICIÓN son muy ALTOS
* Son generalmente DUROS
SI conducen el calor y la electricidad.
* El aire libre :
provoca en superficie CORROSIÓN
*Esta estructura presenta DUCTIBILIDAD y MALEABILIDAD.
EJEMPLOS:
Fe
Ni