par margarita molina Il y a 10 années
1501
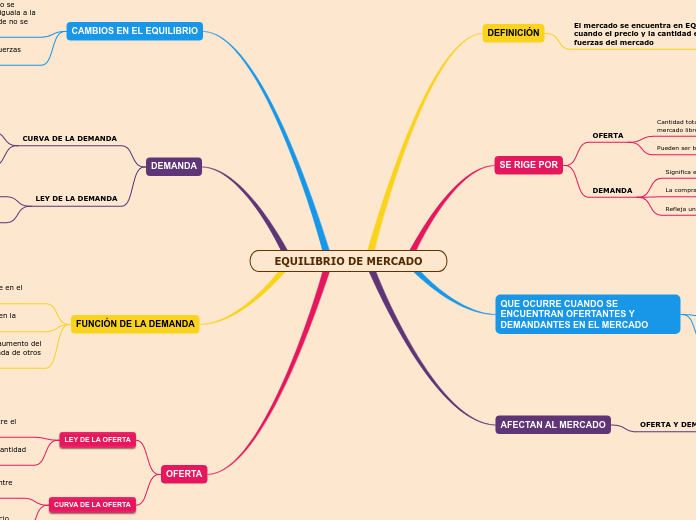
Factore que afectan el equilibrio químico
El principio de Le Châtelier describe cómo un sistema en equilibrio químico responde a cambios en las condiciones externas. Cuando se altera la presión, el equilibrio se desplaza hacia el lado con mayor o menor número de moles dependiendo de si la presión disminuye o aumenta, respectivamente.